
*
Zahteva za preklic dovoljenja Evropske medicinske agencije za uporabo COVID-19 mRNA cepiv
Emer Cooke
Executive Director
European Medicines Agency
Amsterdam
The Netherlands
28. Februar 2021
Spoštovane,
ZA NUJNO OSEBNO POZORNOST :
EMER COOKE
IZVRŠNI DIREKTOR EVROPSKE MEDICINSKE AGENCIJE (EMA)
POSLANO SAMO PO E- POŠTI
Kot zdravniki in znanstveniki načeloma podpiramo uporabo novih medicinskih posegov, ki so ustrezno razviti in uporabljeni in so od bolnika pridobili informirano soglasje. Ta drža vključuje cepiva na enak način kot terapevtska zdravila.
Ugotavljamo, da se po cepljenju predhodno zdravih mlajših posameznikov s cepivom za COVID-19, ki temelji na genetiki, poroča o široki paleti neželenih učinkov. Poleg tega je bilo veliko poročil v medijih po vsem svetu, da so oskrbovanci v domovih za starejše občane zboleli za COVID-19 nekaj dni po cepljenju. Čeprav priznavamo, da so bili ti dogodki lahko, vsak od njih, nesrečna naključja, smo zaskrbljeni, da ni bilo in da še naprej ni zadostnega nadzora nad možnimi vzroki bolezni ali smrti v teh okoliščinah, še posebej pa v odsotnosti pregledov po smrti (obdukcij).
Zlasti se sprašujemo, ali so bila pred odobritvijo Evropske agencije za zdravila (EMA) ustrezno obravnavana glavna vprašanja v zvezi z varnostjo cepiv.
Zelo nujno zahtevamo, da nam EMA posreduje odgovore na naslednja vprašanja:
1. Po intramuskularni injekciji je treba pričakovati, da bodo cepiva na genski osnovi dosegla krvni obtok in se razširjala po vsem telesu [1]. Zahtevamo dokaze, da je bila ta možnost izključena v predkliničnem modelu živali z vsemi tremi cepivi pred odobritvijo za uporabo pri ljudeh s strani EMA.
2. Če takšni dokazi niso na voljo, je treba pričakovati, da bodo cepiva ostala ujeta v obtoku in da jih bodo prevzele endotelijske celice. Obstaja razlog za predpostavko, da se bo to zgodilo zlasti na mestih počasnega pretoka krvi, to je v majhnih žilah in kapilarah [2]. Zahtevamo dokaze, da je bila ta verjetnost izključena v predkliničnem modelu živali z vsemi tremi cepivi pred odobritvijo za uporabo pri ljudeh s strani EMA.
3. Če taki dokazi niso na voljo, je treba pričakovati, da bodo med izražanjem nukleinskih kislin cepiva, peptidi - pridobljeni iz konice beljakovin, predstavljeni prek poti MHC I - poti na luminalni površini celic. Veliko zdravih posameznikov ima CD8-limfocite, ki prepoznajo takšne peptide, ki so lahko posledica predhodne okužbe s COVID-om, pa tudi navzkrižnih reakcij na druge vrste Koronavirusov [3; 4] [5]. Domnevati moramo, da bodo ti limfociti napadli zadevne celice. Zahtevamo dokaze, da je bila ta verjetnost izključena v predkliničnem modelu živali z vsemi tremi cepivi pred odobritvijo za uporabo pri ljudeh s strani EMA.
4. Če taki dokazi niso na voljo, je treba pričakovati, da bo na neštetih mestih po vsem telesu nastala poškodba endotelija s posledičnim sprožanjem koagulacije krvi z aktivacijo trombocitov. Zahtevamo dokaze, da je bila ta verjetnost izključena v predkliničnem modelu živali z vsemi tremi cepivi pred odobritvijo za uporabo pri ljudeh s strani EMA.
5. Če takšni dokazi niso na voljo, je treba pričakovati, da bo to povzročilo padec števila trombocitov, pojav D-dimers v krvi in nešteto ishemičnih lezij po vsem telesu, vključno v možganih, hrbtenjači in srcu. Motnje krvavitve se lahko pojavijo po tej novosti tipa DIC-sindroma (razširjene intravaskularne koagulacije), vključno z drugimi možnostmi kot so močne krvavitve in hemoragične kapi. Zahtevamo dokaze, da so bile vse te možnosti izključene v predkliničnem modelu živali z vsemi tremi cepivi pred odobritvijo za uporabo pri ljudeh s strani EMA.
6. Beljakovinska bodica SARS-CoV-2 se veže na receptor ACE2 na trombocitih, kar povzroči njihovo aktivacijo [6]. O trombocitopeniji so poročali v hudih primerih okužbe z SARS-CoV-2 [7]. O trombocitopeniji so poročali tudi pri cepljenih osebah [8]. Zahtevamo dokaze, da je bila izključena morebitna nevarnost aktivacije trombocitov, ki bi povzročila tudi razširjeno intravaskularno koagulacijo (DIC), pri vseh treh cepivih pred odobritvijo za uporabo pri ljudeh s strani EMA.
7. Širjenje SARS-CoV-2 po svetu je ustvarilo pandemijo bolezni, povezano z mnogimi smrtmi. Vendar v trenutku odobritve cepiv zdravstveni sistemi večine držav niso bili več ogroženi, ker je bil vse večji delež sveta že okužen in se je najhujša pandemija že zniževala. Zato zahtevamo prepričljive dokaze, da je v času, ko je EMA proizvajalcem odobrila pogojno dovoljenje za promet z vsemi tremi cepivi, obstajala dejanska nujna potreba, ki bi upravičevala njihovo odobritev za uporabo pri ljudeh s strani EMA, ki naj bi bila posledica take nujnosti.
Če vsi ti dokazi ne bodo na voljo, zahtevamo, da se odobritev za uporabo cepiv na osnovi genetike, prekliče, dokler EMA ne bo v skladu z načelom skrbnega ravnanja ustrezno obravnavala vseh navedenih vprašanj.
Obstajajo resni pomisleki, vključno z zgoraj opisanimi in drugimi vprašanji, da je bila odobritev cepiva COVID-19 s strani EMA prezgodnja in nepremišljena in da je dajanje cepiv bilo in še vedno je "eksperiment na ljudeh", ki je bil in še vedno je kršitev Nürnberškega zakonika.
Glede na nujnost razmer zahtevamo, da v sedmih dneh odgovorite na to e-pošto in vse naše pomisleke vsebinsko obravnavate. Če se odločite, da se ne boste odzvali na to razumno prošnjo, bomo to pismo javno objavili.
Ta e-pošta je poslana v vednost:
Charles Michel, Predsednik Sveta Evrope
Ursula von der Leyen, Predsednica Evropske Komisije
*
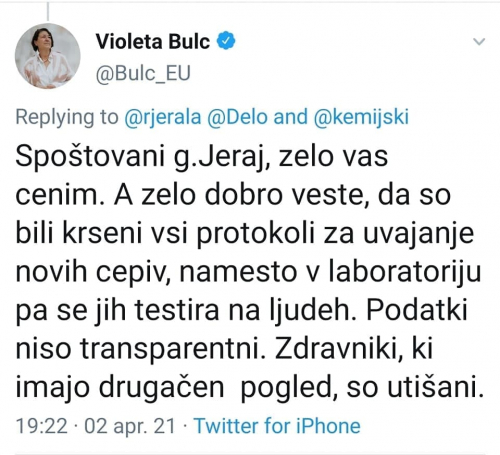
EMA – Europska agencija za lijekove 1. ožujka 2021. primila je originalno pismo preko 100 liječnika i znanstvenika iz 25 država u kojem se opisuju rizici poremećaja krvi od cjepiva COV-19. Preko desetak država suspendiralo je cjepivo AstraZeneca nakon smrti od zgrušavanja i krvarenja, kao što su liječnici i znanstvenici upozorili.
Međutim, 23. ožujka 2021. EMA je odbacila zabrinutost grupe koja se odnosi na “manje” i “rijetke” događaje, zaključivši da je “uspostavljen pozitivan odnos koristi i rizika”.
1. travnja 2021. liječnici i znanstvenici iz 25 zemalja izdali su pismo pobijanja Europskoj agenciji za lijekove (EMA), nakon što je regulator odbacio njihova prethodna upozorenja u vezi s opasnošću od zgrušavanja i krvarenja od COVID-19 cjepiva.
Liječnici i znanstvenici uzvratili su udarac, optužujući EMA da obmanjuje javnost o stvarnom profilu rizika i koristi cjepiva. “Vaš odgovor od 23. ožujka 2021. neuvjerljiv je i neprihvatljiv”, napisali su, napominjući da zabilježeni slučajevi životno opasne cerebralne venske tromboze (CSVT) nakon cijepljenja “predstavljaju samo vrh ogromne sante leda”. Uobičajene reakcije na cijepljenje, uključujući glavobolju, mučninu, zamagljen vid i povraćanje, simptomi su CSVT-a i treba ih odmah procijeniti.
Zgrušavanje i krvarenje nakon cijepljenja također se “mogu očekivati da se povećavaju sa svakim ponovnim cijepljenjem i svakom intervenirajućom izloženošću koronavirusu”, upozorila je skupina. S vremenom „ovo čini ponovljeno cijepljenje i uobičajene koronaviruse opasnim za mlade i zdrave dobne skupine za koje – u odsustvu „cijepljenja“ – COVID-19 ne predstavlja suštinski rizik.
„Takva je stvarna analiza rizika i koristi „cjepiva“ protiv COVIDA-19. Ili EMA-i nedostaje stručnost za predmet da bi uvažila molekularnu znanost ove stvarnosti ili joj nedostaje medicinska etika da bi djelovala u skladu s tim.”
Skupina Doctors for Covid Ethics, koja uključuje profesore imunologije i mikrobiologije, opisala je odgovore EMA-e na njihove zabrinutosti kao “neznanstvene”, “nejasne” i nedostajuće vjerodostojnosti. Ponudili su suradnju s agencijom radi ublažavanja rizika od cijepljenja i kršenja etike, uključujući pomoć EMA-i da “izradi fokusirani plan farmakovigilancije”.
Skupina je upozorila da nastavak primjene neadekvatnih cjepiva protiv COVIDA-19 zasnovanih na genima predstavlja opasno medicinsko eksperimentiranje, čiji “istinski rizici daleko premašuju bilo kakvu teorijsku korist”, što odražava “ozbiljna kršenja medicinske etike i medicinskih prava građana”.
“Obmanjivanje populacije da prihvate istraživačke agense, poput genetskih cjepiva
COVID-19, ili njihovo prisiljavanje putem putovnica cjepiva, “predstavlja jasna i gruba kršenja Nürnberškog zakonika”, upozoravaju oni.
Pismo je upućeno Emer Cookeu, izvršnom direktoru EMA-e, a kopirano je odvjetniku Reineru Fuellmichu, Charlesu Michelu, predsjedniku Vijeća Europe i Ursuli von der Leyen, predsjednici Europske komisije.
Vezu do pisma pobijanja liječnika za Covid Ethics na EMA (1. travnja 2021.) možete pogledati ovdje.
Link na pismo EMA-e liječnicima za etiku Covid (23. ožujka 2021.) – Link.
Liječnici za Covid Ethics skupina je od preko 100 liječnika i znanstvenika iz 25 zemalja.
Web: https://doctors4covidethics.medium.com
Twitter: https://twitter.com/Drs4CovidEthics
Za komentar se obratite prof. Dr. Sucharit Bhakdi: sucharit.bhakdi@gmx.de ili izvanrednom profesoru Michaelu Palmeru: mpalmer@uwaterloo.ca
Originalno pismo liječnika za etiku Covid EMA-i (dostavljeno 1. ožujka 2021.) pogledajte na linku.
HITNO OTVORENO PISMO LIJEČNIKA I ZNANSTVENIKA EUROPSKOJ AGENCIJI ZA LIJEKOVE U VEZI SA ZABRINUTOŠĆU ZA SIGURNOST CJEPIVA COVID-19
Europska agencija za lijekove
Emer Cooke, izvršni direktor
Amsterdam
Nizozemska
28. veljače 2021
Poštovani,
Kao liječnici i znanstvenici, načelno podržavamo upotrebu novih medicinskih intervencija koje se na odgovarajući način razvijaju i primjenjuju, dobivši informirani pristanak pacijenta. Ovo stajalište obuhvaća cjepiva na isti način kao i terapeutike.
Primjećujemo da se izvještava o širokom rasponu nuspojava nakon cijepljenja prethodno zdravih mlađih pojedinaca cjepivima protiv COVIDA-19 na genskoj osnovi. Štoviše, brojni su izvještaji medija iz cijelog svijeta o domovima za njegu koje je COVID-19 udario u roku od nekoliko dana od cijepljenja stanovnika. Iako prepoznajemo da su se ove pojave mogle dogoditi nesretnom slučajnosti, zabrinuti smo što je bilo, a i dalje se vrši, neodgovarajući nadzor mogućih uzroka bolesti ili smrti u tim okolnostima, a posebno u odsustvu post-mortem pregleda.
Posebno se pitamo jesu li glavna pitanja u vezi sa sigurnošću cjepiva na odgovarajući način riješena prije nego što ih je odobrila Europska agencija za lijekove (EMA).
Kao vrlo hitno, ovim putem tražimo da nam EMA dostavi odgovore na sljedeća pitanja:
- Nakon intramuskularne injekcije, mora se očekivati da će cjepiva na genskoj osnovi doći do krvotoka i širiti se tijelom [1]. Zahtijevamo dokaze da je ta mogućnost isključena u predkliničkim životinjskim modelima sa sva tri cjepiva prije nego što ih je EMA odobrila za upotrebu na ljudima.
- Ako takvi dokazi nisu dostupni, mora se očekivati da će cjepiva ostati zarobljena u cirkulaciji i da će ih endotelne stanice apsorbirati. Postoji razlog za pretpostaviti da će se to dogoditi posebno na mjestima usporenog protoka krvi, tj. u malim žilama i kapilarima [2]. Zahtijevamo dokaze da je ta vjerojatnost isključena u predklinički životinjski modeli sa sva tri cjepiva prije nego što ih je EMA odobrila za upotrebu na ljudima.
- Ako takvi dokazi nisu dostupni, mora se očekivati da će tijekom ekspresije nukleinskih kiselina cjepiva peptidi izvedeni iz proteina klas biti predstavljeni putem MHC I – puta na luminalnoj površini stanica. Mnoge zdrave osobe imaju CD8-limfocite koji prepoznaju takve peptide, što je možda posljedica prethodne infekcije COVID-om, ali i križnih reakcija s drugim vrstama koronavirusa [3; 4] [5]. Moramo pretpostaviti da će ovi limfociti izvršiti napad na odgovarajuće stanice. Zahtijevamo dokaze da je ta vjerojatnost isključena u predkliničkim životinjskim modelima sa sva tri cjepiva prije nego što ih je EMA odobrila za upotrebu na ljudima.
- Ako takvi dokazi nisu dostupni, mora se očekivati da će doći do oštećenja endotela s naknadnim pokretanjem koagulacije krvi aktivacijom trombocita na bezbrojnim mjestima u tijelu. Zahtijevamo dokaze da je ta vjerojatnost isključena u predkliničkim životinjskim modelima sa sva tri cjepiva prije nego što ih je EMA odobrila za upotrebu na ljudima.
- Ako takvi dokazi nisu dostupni, mora se očekivati da će to dovesti do pada broja trombocita, pojave D-dimera u krvi i do bezbrojnih ishemijskih lezija u cijelom tijelu, uključujući mozak, leđnu moždinu i srce . Poremećaji krvarenja mogu se pojaviti nakon ove nove vrste DIC sindroma, uključujući, između ostalih mogućnosti, obilna krvarenja i hemoragični moždani udar. Zahtijevamo dokaze da su sve te mogućnosti isključene u predkliničkim životinjskim modelima sa sva tri cjepiva prije nego što ih je EMA odobrila za upotrebu na ljudima.
- SARS-CoV-2 bjelančevinasti spike veže se na ACE2 receptor na trombocitima, što rezultira njihovom aktivacijom [6]. Trombocitopenija je zabilježena u teškim slučajevima infekcije SARS-CoV-2 [7]. Trombocitopenija je također zabilježena u cijepljenih osoba [8]. Zahtijevamo dokaze da je potencijalna opasnost od aktivacije trombocita koja bi također dovela do diseminirane intravaskularne koagulacije (DIC) isključena sa sva tri cjepiva prije nego što ih je EMA odobrila za upotrebu na ljudima.
- Širenje SARS-CoV-2 širom svijeta stvorilo je pandemiju bolesti povezanu s mnogim smrtnim slučajevima. Međutim, do trenutka razmatranja zahtjeva za odobravanje cjepiva, zdravstveni sustavi većine zemalja više nisu bili pod neposrednom prijetnjom da budu preopterećeni jer je sve veći dio svijeta već zaražen, a najgora pandemija već je utihnula. Slijedom toga, zahtijevamo konačne dokaze da je stvarna nužda postojala u vrijeme kada je EMA izdala uvjetno odobrenje za promet proizvođačima sva tri cjepiva, kako bi opravdala njihovo odobrenje za upotrebu od strane EMA-e, navodno zbog takve nužde.
Ako svi takvi dokazi ne budu dostupni, tražimo da se povuče odobrenje za upotrebu genskih cjepiva sve dok EMA ne riješi sve gore navedene probleme na odgovarajući način.
Postoje ozbiljne zabrinutosti, uključujući, ali ne ograničavajući se na gore navedene, da je odobrenje cjepiva COVID-19 od strane EMA bilo preuranjeno i nepromišljeno te da je davanje cjepiva predstavljalo i još uvijek predstavlja “ljudsko eksperimentiranje”, i dalje krši Nürnberški zakonik.
S obzirom na hitnost situacije, tražimo da odgovorite na ovu e-poštu u roku od sedam dana i da suštinski riješite sve naše nedoumice. Ako odlučite ne udovoljiti ovom razumnom zahtjevu, objavit ćemo ovo pismo.
Ova e-pošta kopirana je na:
- Charles Michel, predsjednik Vijeća Europe
- Ursula von der Leyen, predsjednica Europske komisije.
Liječnici i znanstvenici mogu potpisati otvoreno pismo slanjem svog imena, kvalifikacija, područja stručnosti, zemlje i bilo koje organizacije koju žele citirati na Doctors4CovidEthics@protonmail.com
Reference
[1] Hassett, K.J .; Benenato, K.E .; Jacquinet, E .; Lee, A.; Woods, A.; Južakov, O.; Himansu, S .; Određivanje, J .; Geilich, B.M .; Ketova, T .; Mihai, C .; Lynn, A .; McFadyen, I .; Moore, M.J .; Senn, J.J .; Stanton, M.G .; Almarsson, Ö .; Ciaramella, G. i Brito, L. A. (2019). Optimizacija nanočestica lipida za intramuskularno davanje mRNA cjepiva, Molekularna terapija. Nukleinske kiseline 15: 1–11.
[2] Chen, Y. Y .; Syed, A.M .; MacMillan, P.; Rocheleau, J. V. i Chan, W. C. W. (2020). Brzina protoka utječe na unos nanočestica u endotelne stanice, napredni materijali 32: 1906274.
[3] Grifoni, A .; Weiskopf, D .; Ramirez, S. I .; Mateus, J .; Dan, J.M .; Moderbacher, C.R .; Rawlings, S.A .; Sutherland, A .; Premkumar, L .; Jadi, R. S. i suradnici (2020). Ciljevi odgovora T stanica na koronavirus SARS-CoV-2 u ljudi s bolešću COVID-19 i neeksponiranim osobama, stanica 181: 1489-1501.e15.
[4] Nelde, A .; Bilich, T .; Heitmann, J.S .; Maringer, Y .; Salih, H.R .; Roerden, M .; Lübke, M .; Bauer, J .; Rieth, J .; Wacker, M .; Peter, A .; Hörber, S.; Traenkle, B .; Kaiser, P. D.; Rothbauer, U .; Becker, M .; Junker, D.; Krause, G .; Strengert, M .; Schneiderhan-Marra, N .; Templin, M.F .; Joos, T.O .; Kowalewski, D.J .; Stos-Zweifel, V .; Fehr, M .; Rabsteyn, A .; Mirakaj, V .; Karbach, J .; Jäger, E .; Graf, M .; Gruber, L.-C .; Rahfalski, D.; Preuß, B .; Hagelstein, I .; Märklin, M .; Bakchoul, T .; Gouttefangeas, C .; Kohlbacher, O .; Klein, R .; Stevanović, S .; Rammensee, H.-G. i Walz, J. S. (2020). Peptidi izvedeni iz SARS-CoV-2 definiraju heterologno i COVID-19-inducirano prepoznavanje T stanica, imunologija Nature.
[5] Sekine, T .; Perez-Potti, A .; Rivera-Ballesteros, O .; Strålin, K .; Gorin, J.-B .; Olsson, A .; Llewellyn-Lacey, S.; Kamal, H .; Bogdanović, G .; Muschiol, S. i suradnici (2020). Robusna imunost na T stanice u osoba koje oporavljaju s asimptomatskim ili blagim COVID-19, stanica 183: 158–168.e14.
[6] Zhang, S.; Liu, Y .; Wang, X .; Yang, L .; Li, H .; Wang, Y .; Liu, M .; Zhao, X .; Xie, Y .; Yang, Y .; Zhang, S.; Ventilator, Z .; Dong, J .; Yuan, Z .; Ding, Z .; Zhang, Y. i Hu, L. (2020). SARS-CoV-2 na trombocite veže ACE2 za pojačavanje tromboze u COVID-19, Časopis za hematologiju i onkologiju 13: 120.
[7] Lippi, G .; Plebani, M. i Henry, B. M. (2020). Trombocitopenija je povezana s teškim infekcijama koronavirusnom bolešću 2019 (COVID-19): Meta-analiza, Clin. Chim. Acta 506: 145–148.
[8] Grady, D. (2021). Nekoliko je primatelja cjepiva Covid razvilo poremećaj rijetke krvi, The New York Times, 8. veljače 2021.
S poštovanjem,
Seznam podpisanikov je na strani:
https://www.logicno.com/politika/ema-european-medicines-agency-obmanjuje-javnost-tvrde-lijecnici-i-znanstvenici-iz-25-drzava.html
* * *
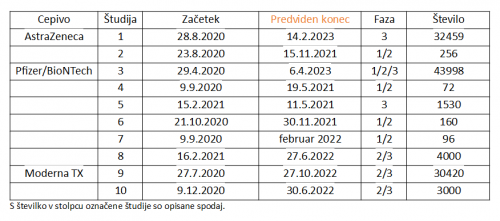
Few days ago we have received an tabel with numbers of all side effects of new vaccines against new corona virus / covid-19 disease. The numbers are said to be collected from your official side and are valid for EU on 13th of April 2021. For any case we would like to check that numbers, so we are asking you the falloving:
- what is the sum of all side effects for all c-19 vaccines in EU?
- what is the sum of all death cases that are confirmed to be caused by new C-19 vaccines?
- what is the sum of all death cases that are suspected to be caused by new C-19 vaccines, but not confirmed?
Thank you for your reply,
Best regards,
Jure Pogačnik, univ. dipl. iur. 27.4. 2021
In a public comment to the CDC, molecular biologist and toxicologist Dr. Janci Chunn Lindsay, Ph.D., called to immediately halt Covid vaccine production and distribution. Citing fertility, blood-clotting concerns (coagulopathy), and immune escape, Dr. Lindsay explained to the committee the scientific evidence showing that the coronavirus vaccines are not safe.
On April 23, 2021, the CDC’s Advisory Committee on Immunization Practices held a meeting in Atlanta, Georgia. The focus of this ACIP meeting was blood clotting disorders following Covid vaccines. Dr. Janci Chunn Lindsay spoke to the CDC during the time set aside for public comment.
The censorship on social media in particular and the internet in general is relentless. Here is a slightly edited, annotated censorship-proof transcript of Dr. Janci Chunn Lindsay’s 3-minute comment.
You can listen to her testimony on YouTube here (for now, anyway. If this link goes viral, YouTube will likely censor it).
Molecular Biologist and Toxicologist Calls to Halt Covid Vaccine
Hi, my name is Dr. Janci Chunn Lindsay. I hold a doctorate in biochemistry and molecular biology from the University of Texas, and have over 30 years of scientific experience, primarily in toxicology and mechanistic biology.
In the mid-1990s, I aided the development of a temporary human contraceptive vaccine which ended up causing unintended autoimmune ovarian destruction and sterility in animal test models. Despite efforts against this and sequence analyses that did not predict this.
I strongly feel that all the gene therapy vaccines must be halted immediately due to safety concerns on several fronts.
Janci Chunn Lindsay: Covid vaccines could induce cross-reactive antibodies to syncytin, and impair fertility as well as pregnancy outcomes
First, there is a credible reason to believe that the Covid vaccines will cross-react with the syncytin and reproductive proteins in sperm, ova, and placenta, leading to impaired fertility and impaired reproductive and gestational outcomes.
Respected virologist Dr. Bill Gallaher, Ph.D., made excellent arguments as to why you would expect cross reaction. Due to beta sheet conformation similarities between spike proteins and syncytin-1 and syncytin-2.
I have yet to see a single immunological study which disproves this. Despite the fact that it would literally take the manufacturers a single day to do these syncytin studies to ascertain this [once they had serum from vaccinated individuals]. It’s been over a year since the assertions were first made that this [the body attacking its own syncytin proteins due to similarity in spike protein structure] could occur.
Pregnancy losses reported to VAERS lead to demand to halt Covid vaccine
We have seen 100 pregnancy losses reported in VAERS as of April 9th. And there have [also] been reports of impaired spermatogenesis and placental findings from both the natural infection, vaccinated, and syncytin knockout animal models that have similar placental pathology, implicating a syncytin-mediated role in these outcomes.
Additionally, we have heard of multiple reports of menses irregularities in those vaccinated. These must be investigated.
We simply cannot put these [vaccines] in our children who are at .002% risk for Covid mortality, if infected, or any more of the child-bearing age population without thoroughly investigating this matter.
[If we do], we could potentially sterilize an entire generation. Speculation that this will not occur and a few anecdotal reports of pregnancies within the trial are not sufficient proof that this is not impacting on a population-wide scale.
Covid vaccine causes blood disorders
Secondly, all of the gene therapies [Covid vaccines] are causing coagulopathy. [Coagulopathy when the body’s blood clotting system is impaired.] This is not isolated to one manufacturer. And this is not isolated to one age group.
As we are seeing coagulopathy deaths in healthy young adults with no secondary comorbidities.
There have been 795 reports related to blood clotting disorders as of April 9th in the VAERS reporting system, 338 of these being due to thrombocytopenia.
There are forward and backward mechanistic principles for why this is happening. The natural infection is known to cause coagulopathy due to the spike protein. All gene therapy vaccines direct the body to make the spike protein. Zhang et al in [a scientific paper published in the Journal of Hematology & Oncology] in September 2020 showed that if you infuse spike protein into mice that have humanized ACE-2 receptors on blood platelets that you also get disseminated thrombosis.
Spike protein incubated with human blood in vitro also caused blood clot development which was resistant to fibrinolysis. [Fibrinolysis is the body’s process of breaking down blood clots]. The spike protein is causing thrombocytic events, which cannot be resolved through natural means. And all vaccines must be halted in the hope that they can be reformulated to guard against this adverse effect.
Third, there is strong evidence for immune escape—
At this point in her oral testimony, Dr. Janci Chunn Lindsay was interrupted by a man’s voice: “Thank you for your comment, your time has expired.”
I reached out to Dr. Janci Chunn Lindsay to find out what else she had wanted to share with ACIP, in addition to her concerns over fertility and blood-clotting disorders. She sent me back her third point, which she submitted as written testimony.
Third, there is strong evidence for immune escape, and that inoculation under pandemic pressure with these leaky vaccines is driving the creation of more lethal mutants that are both newly infecting a younger age demographic, and causing more Covid-related deaths across the population than would have occurred without intervention. That is, there is evidence that the vaccines are making the pandemic worse.
It is clear that we are seeing a temporal immune depression immediately following the inoculations [see World Meter Global Covid deaths counts following inoculation dates] and there are immunosuppressive regions on spike proteins, as well as Syn-2, that could be likely causing this, through a T-cell mediated mechanism. If we do not stop this vaccine campaign until these issues can be investigated, we may see a phenomenon such as we see in chickens with Marek’s disease.
We have enough evidence now to see a clear correlation with increased Covid deaths and the vaccine campaigns. This is not a coincidence. It is an unfortunate unintended effect of the vaccines. We simply must not turn a blind eye and pretend this is not occurring. We must halt all Covid vaccine administration immediately, before we create a true pandemic that we cannot reign in.
MIT scientist also concerned about blood-clotting, fertility issues
Stephanie Seneff, Ph.D., an expert in protein synthesis, believes that Dr. Lindsay’s hypothesis is correct. “I absolutely share these concerns,” Dr. Seneff, who is a senior research scientist at MIT, wrote to me in a sobering email.
“The potential for blood clotting disorders and the potential for sterilization are only part of the story. There are other potential long-term effects of these vaccines as well, such as autoimmune disease and immune escape, whereby the vaccines administered to immune-compromised people accelerate the mutation rate of the virus so as to render both naturally acquired and vaccine-induced antibodies no longer effective.”
Like Dr. Lindsay, Dr. Seneff believes we need to immediately halt Covid vaccine campaigns. “This massive clinical trial on the general population could have devastating and irreversible effects on a huge number of people,” Seneff explains.
Despite these fertility and blood disorder concerns, the CDC panel voted last Friday to resume the use of the Johnson and Johnson vaccine. They did, however, suggest an FDA warning label be added. Their argument against halting Covid vaccination? The CDC believes the benefits outweigh the risks.
https://www.jennifermargulis.net/halt-covid-vaccine-research-scientist-urges-cdc/
*
By Doctors for COVID Ethics
Global Research, April 02, 2021
Rebuttal Letter to European Medicines Agency (EMA) from Doctors for COVID Ethics
From Doctors for Covid Ethics
Emer Cooke, Executive Director, European Medicines Agency, Amsterdam, The Netherlands
April 1st, 2021
Ladies and Gentlemen,
FOR THE URGENT PERSONAL ATTENTION OF: EMER COOKE, EXECUTIVE DIRECTOR OF THE EUROPEAN MEDICINES AGENCY
We acknowledge receipt of your March 23 reply to our letter dated February 28, seeking reassurance that foreseeable risks of gene-based COVID-19 “vaccines” had been ruled out in animal trials prior to human use. Our concerns arise from multiple lines of evidence, including that the SARS-CoV-2 “spike protein” is not a passive docking protein, but its production is likely to initiate blood coagulation via multiple mechanisms.
Regrettably, your reply of March 23 is unconvincing and unacceptable. We are dismayed that you choose to respond to our request for crucially important information in a dismissive and unscientific manner. Such a cavalier approach to vaccine safety creates the unwelcome impression that the EMA is serving the interests of the very pharmaceutical companies whose products it is your pledged duty to evaluate. The evidence is clear that there are some serious adverse event risks & that a number of people, not at risk from SARS-CoV-2, have died following vaccination.
1. You concede that the “vaccines”, which are more accurately described as investigational gene-based agents, enter the bloodstream but you can obviously provide no quantitative data. In the absence of the latter, any scientific assessment you purport to have undertaken lacks foundation.
2. Your statement that non-clinical studies do not indicate any detectable uptake of the vaccines into endothelial cells lacks credibility. We demand to see the scientific evidence. If not available, it must be assumed that endothelial cells are targeted.
3. Auto-attack could not have been excluded in animals unless they had been immunologically primed beforehand. We demand evidence that such experiments had been performed. Similar experiments have been undertaken before with previous, unsuccessful candidate vaccines, and fatal, antibody-dependent enhancement of disease was observed.
4. We requested scientific evidence, not a vague description of what was purportedly seen in non-valid animal experiments. Your cursory mention of laboratory findings in humans is cynical. In view of the plausible connection between production of spike protein and the emergence of thromboembolic serious adverse events (SAEs), we demand to see the results of D-dimer determinations. As you are aware, D-dimer is a very good test as an aid to diagnose thrombosis.
After delivery of our letter to you on March 1, events followed that debunk your response to our last three queries to an extent that can only be termed embarrassing. As we feared, severe and fatal coagulopathies occurred in young individuals following “vaccination”, leading 15 countries to suspend their AZ-“vaccination” program. An official investigation by the EMA into the cases of afflicted younger individuals followed, the results of which were announced by the WHO on March 17, 2021, stating: “At this time, WHO considers that the benefits of the AstraZeneca vaccine outweigh its risks and recommends that vaccinations continue.”
What was this decision based upon? The WHO is not a competent body for formally evaluating drug safety. That is explicitly the role of the agency you lead.
In your press release, you disclosed the following information to support your conclusion. You had scrutinized data on two mortally dangerous conditions that had followed within 14 days of “vaccination”: DIC, disseminated intravascular coagulation; and CSVT, cerebral sinus vein thrombosis. 5 DIC and 18 CSVT were on record, with a total death toll of 9. Most cases were 55 year-old individuals. 5 DIC and 12 CSVT were under 50 years of age. None were reported as having had serious pre-existing illness.
You stated numbers that “normally” would be expected : DIC <1, CSVT 1.3.
Consequently, for these very rare conditions, a link to vaccination could not entirely be dismissed. However, given that 20 million individuals had been “vaccinated”, the benefits were deemed to far outweigh the risks.
But in fact, your Press Release rendered it glaringly apparent that the AZ-“vaccine” does have the potential to trigger intravascular coagulation, that the true risks far outweigh any theoretical benefits, and that any authority with the slightest sense of responsibility must suspend its further use.
1. Regard your incidence numbers for
CSVT : 12 versus 1.3.
A 9-fold increase is beyond the range of coincidence.
DIC : 5 versus <1.
As we hope you know, DIC neveroccurs out of the blue in healthy individuals. The incidence should not be stated as
ACCORDINGLY, THE DIC CASES REPRESENT CONCLUSIVEEVIDENCE THAT THE AZ-VACCINE ALONE CAN TRIGGER INTRAVASCULAR COAGULATION .
2. Assume that 10 million recipients of the “vaccine” were
The pandemic hit around 60 million individuals
During the first 6 months it reportedly claimed 52 lives of individuals without pre-existing illness (See this)
Because of the unreliability of PCR testing and because of the completely novel way that deaths ‘with covid19’ are determined, the value of 52 is an over-estimate of the real burden of disease, further weakening your already-inadequate claim for risk-benefit.
How, then, can you declare that the benefits of vaccination far outweigh the risks? We demand your reply supported by facts and figures that we will convey to the public.
3. Further considerations expose the truly frightful dimensions of your irresponsible assertion.
CSVT, cerebral venous thrombosis, is always a life-threatening condition that demands immediate medical attention. The number of cases you conceded had occurred can represent just the tip of a huge iceberg. As you must know, the most common symptoms of CSVT are piercing headache, blurred vision, nausea and vomiting. In severe cases, stroke-like symptoms occur including impairment of speech, vision and hearing, body numbness, weakness , decreased alertness and loss of motoric control.
Surely, you are not oblivious to the fact that countless individuals suffered from precisely such symptoms directly following “vaccinations” with all the experimental gene-based agents.
Clot formation in deep leg veins can lead to lethal pulmonary embolisms. Surely you must know that peripheral venous thromboses have repeatedly been reported following “vaccinations” with all the experimental gene-based agents
Microthromboses in the lung vasculature can lead to misdiagnosis of pneumonia. In combination with false-positive PCR (with high cycle thresholds), these will then be registered as COVID 19 cases. Surely you must know that this scenario has probably repeatedly taken place following “vaccinations” with all the experimental gene- based agents.
In all events, extensive thrombi formation can lead to consumption of platelets and coagulation factors, resulting in hemorrhagic diathesis and bleeding at all possible locations. Surely you must know that profuse skin bleedings have repeatedly been observed following “vaccinations” with all the experimental gene-based agents.
Given that there is a mechanistically plausible explanation for these thromboembolic adverse drug reactions (TE ADRs), namely that the gene-based products induce human cells to manufacture potentially pro-thrombotic spike protein, the reasoned & responsible assumption must now be that this may be a class effect. In other words, the dangers must be ruled out for all emergency-authorised gene-based vaccines, not merely the AZ product.
We urge you to adopt this stance unless and until there is data providing high clinical confidence to the contrary. We are very willing to liaise with the Agency in order to help craft a focussed pharmacovigilance plan to accomplish this goal. With the above in mind, we hope you are aware that all thrombotic events can be rapidly diagnosed by measurement of D-Dimers in blood. And that good medical practice imperatively demands that attempts are undertaken to diagnose CSVT in any and every patient, young or old, presenting with the typical signs and symptoms following “vaccination”.
Given the potential for adverse effects, potentially fatal ones, it is completely inappropriate and unacceptable that EMA permits these products, which hold only emergency use authorisations, to be administered to younger (<60y) people who are healthy, as they are at unmeasurable risks from SARS-CoV-2.
Not to make this explicit is, in our view, a reckless stance to have taken in the first place and doubly so now.
Of equal importance, you are bound by duty to investigate whether reasons exist for the waves of deaths that have occurred following “vaccination” of elderly residents in care and senior homes. Or are you asserting that dangers of “vaccine”-derived thrombotic events are limited to younger individuals? If not, restricting their use solely in one age group — as decided upon in Germany — equates with nothing less than monstrous, condoned genocide of the other.
In closing, failure to inform “vaccine” recipients of the risks and negligible benefits outlined here represents serious violations of medical ethics and citizens’ medical rights. Those violations are especially grave as all the risks we describe can be expected to increase with each re-vaccination, and each intervening coronavirus exposure. This renders both repeated vaccination and common coronaviruses dangerous to young and healthy age groups, for whom — in the absence of “vaccination” — COVID-19 poses no substantive risk.
Such is the real risk-benefit analysis of the COVID-19 “vaccines”. Either the EMA lacks the subject-matter expertise to appreciate the molecular science of this reality, or it lacks the medical ethics to act accordingly.
At best, we regard the EMA’s complacent stance on vaccine dangers to be symptomatic of the fact that, under the prevailing politico-medical response to COVID-19, medical ethics has migrated from the consulting room to a geopolitical stage. Faced with a medical problem, mass-medical intervention has seen the practice of medicine taken from doctors’ hands.In this politicized context, corporate and political actors may consider themselves free from ethical constraints, operating unbound by a medical code of ethics, unlike medical doctors. All actors, however, are bound by the Nuremberg Code.
The Nuremberg Code prohibits human experimentation of the very kind being endorsed and defended by the EMA. Even under the terms of their own original FDA authorization, COVID-19 vaccines are deemed “investigational” and their recipients “human subjects”, who are, by definition, entitled to informed consent. See this.
Misleading populations into accepting investigational agents such as the gene-based COVID-19 “vaccines”, or coercing them through “vaccine passports”, constitutes clear and egregious violations of the Nuremberg Code. The Nuremberg Code mandates voluntary informed consent “without the intervention of any element of force, fraud, deceit [or] duress”. See this.
In other words, citizens have the right under the Nuremberg Code and related protections not to be subject involuntarily to medical experiments. It is clear that these experimental agents should be CONTRA-INDICATED in individuals not at elevated risk of serious illness & death if infected by SARS-CoV-2. Furthermore, the use of the experimental agents must also be withheld in the elderly population until a risk-benefit assessment has been properly conducted. In any event, the vaccine label must be revised to reflect the recently emerged serious adverse events addressed here.
We remind the EMA that Nuremberg violations constitute crimes against humanity under the Geneva Convention. Crimes against humanity are deemed “the worst atrocities known to mankind”, and are prosecuted under the Rome Statute of the International Criminal Court. See this.
Given the hundreds of millions and eventually billions of people who may be coerced into accepting these agents, the EMA, in persistently shrinking from open debate and the truth, will be seen by lawyers and historians as having actively assisted in crimes against humanity, with the full weight of the implications to all involved. We demand thatyou engage openly with us to ensure that the public have an objective understanding of the clinical risk profile of these gene-based interventions.
You understand that coercive pressure is being placed on citizens to receive COVID-19 vaccines, which are experimental medical treatments. Your responsibility to those citizens includes ensuring that they are informed of the adverse event risks of every such treatment. To date you have failed to do so, and have instead misled the public on the reality of the “vaccines’” risk-benefit profile.
If you continue to conceal the truth, efforts will be made to bring this to light and to see that justice is done. For the sake of the injured and the dead, and to protect further lives from similar fates.
Notice
For the avoidance of doubt, if your regulatory body does not immediately suspend its “emergency” recommendation of potentially dangerous inadequately tested gene-based “vaccines”, while the matters which we have highlighted to you are properly investigated, we hereby put the European Medicines Agency on notice of being complicit in medical experimentation, in violation of the Nuremberg Code, which thereby constitutes the commission of crimes against humanity.
Furthermore, it is your indirigible duty as a regulatory body to ensure that all doctors worldwide are advised that they are taking part in medical experimentation via “vaccination” programmes, whether wittingly or unwittingly, with all the legal and ethical obligations that such involvement entails.
This email is copied to the lawyer Reiner Fuellmich. It is also copied to Charles Michel, President of the Council of Europe, and to Ursula von der Leyen, President of the European Commission.
Yours faithfully,
Vir: https://home.solari.com/rebuttal-letter-to-european-medicines-agency-ema-from-doctors-for-covid-ethics/
*
https://www.globalresearch.ca/doctors-scientists-write-european-medicines-agency-warning-covid-19-vaccine-dangers/5739515
*
mRNA cepivo povzroči smrt telesnih celic (apoptosis) : https://odysee.com/@shortXXvids:e/Dr-VS-K-why-m-RNA-vacine-different:2?src=open&r=BWSeHJ8asYoo4uRLsWhCb8D17qQ2xW22&fbclid=IwAR0KJ1_GHe6ea7VDbXafSbcMk1eajvL6g22jnV6he7Ggnyl3FvOHY20savE
*
Znanstvenici – istraživači i “Frontline doctors pozivaju” CDC da zaustavi sva Covid cjepiva
U javnom komentaru CDC-u, molekularni biolog i toksikolog dr. Janci Chunn Lindsay, dr. sc., pozvala je da odmah zaustavi proizvodnju i distribuciju cjepiva za Covid. Pozivajući se na plodnost, zabrinutost za zgrušavanje krvi (koagulopatija) i imunološki bijeg, dr. Lindsay je objasnila odboru znanstvene dokaze koji pokazuju da cjepiva protiv koronavirusa nisu sigurna.
23. travnja 2021. Savjetodavni odbor CDC-a za imunizacijske prakse održao je sastanak u Atlanti u državi Georgia. Fokus ovog ACIP sastanka bili su poremećaji zgrušavanja krvi nakon Covid cjepiva. Doktor Janci Chunn Lindsay razgovarala je s CDC-om tijekom vremena određenog za javnu raspravu. Cenzura na društvenim medijima posebno i interneta u cjelini je nemilosrdna. Evo blago uređenog, s komentarom, transkripta koji je otporan na cenzuru, trominutnog komentara dr. Janci Chunn Lindsay.
Njezino svjedočenje na YouTubeu možete slušati ovdje. (za sad, YouTube će ju vjerojatno cenzurirati).
Dr. Janci Chunn Lindsay – CDC ACIP public comment – April 23, 2021
MOLEKULARNI BIOLOG I TOKSIKOLOG POZIVA NA ZAUSTAVLJANJE COVID CJEPIVA
Dr. sc. Janci Chunn Lindsay je doktor znanosti iz toksikologije i molekularne biologije za usluge podrške toksikologiji, LLC . Doktorirala je iz biokemije i molekularne biologije na Fakultetu za biomedicinske znanosti Sveučilišta u Teksasu, dr. Anderson Cancer Center-Houston. Doktor Lindsay ima veliko iskustvo u analizi molekularnog profila farmakoloških odgovora. Njezina ekspertiza usredotočena je na procjenu složene dinamike toksičnosti, poput farmakologije toksikanata, puta izloženosti, metabolizma domaćina i naknadnih staničnih učinaka koji se odnose na doprinos specifičnih tvari oštećenju, zdravlju i riziku od plodnosti te ljudskim bolestima.
Kaže tako dr. Lindsay:
„Sredinom devedesetih pomogala sam razvoju privremenog cjepiva za ljudsku kontracepciju koje je na kraju prouzročilo nenamjerno autoimuno uništavanje jajnika i sterilnost u modelima za ispitivanje na životinjama. Unatoč naporima protiv toga i analizama sekvenci koje to nisu predvidjele. Čvrsto smatram da se sva cjepiva za gensku terapiju moraju odmah zaustaviti zbog sigurnosnih razloga na nekoliko frontova.“
COVID CJEPIVA MOGU INDUCIRATI UNAKRSNA REAKTIVNA ANTITIJELA NA SINCITIN, TE UMANJITI PLODNOST KAO I ISHOD TRUDNOĆE
Prvo, postoji vjerodostojan razlog za vjerovanje da će Covid cjepiva međusobno reagirati sa sincitinom i reproduktivnim proteinima u spermi, jajnim ćelijama i posteljici, što će dovesti do oštećenja plodnosti i oštećenja reproduktivnih i gestacijskih ishoda.
Ugledni virolog dr. sc. Bill Gallaher, iznio je izvrsne argumente zašto biste očekivali unakrsnu reakciju. Zbog sličnosti konformacije beta lista između proteina klasova i sincitina-1 i sincitina-2. Tako laže dr. Gallaher:
„Još nisam vidio niti jednu imunološku studiju koja to opovrgava. Unatoč činjenici da bi proizvođačima doslovno trebao jedan dan da provedu ove studije sincitina kako bi to utvrdili [nakon što su dobili serum od cijepljenih osoba]. Prošlo je više od godinu dana otkako su prvi put izrečene tvrdnje da se to [tijelo koje napada vlastite proteine sincitina zbog sličnosti u strukturi proteina klasova] može dogoditi. „
GUBITAK TRUDNOĆE PRIJAVLJEN VAERS-U DOVODI DO POTRAŽNJE ZA ZAUSTAVLJANJEM COVID CJEPIVA
Zabilježili smo 100 gubitka trudnoće prijavljene u VAERS-u od 9. travnja. A bilo je (također) izvješća o oštećenjima spermatogeneze i nalazima posteljice od prirodne infekcije, cijepljenih i nokaut životinja na sincitin modelima koji imaju sličnu patologiju posteljice, što implicira ulogu posredovanu sincitinom u tim ishodima. Uz to, čuli smo za višestruka izvješća o nepravilnostima menstruacije kod cijepljenih. To se mora istražiti.
Jednostavno ne možemo staviti ova (cjepiva) svojoj djeci koja imaju 0,002% rizika za smrtnost od Covida, ako su zaraženi, ili bilo kojoj drugoj populaciji u rodnoj dobi, bez temeljitog istraživanja ove stvari.
(Ako to učinimo), potencijalno bismo mogli sterilizirati cijelu generaciju. Špekulacije da se to neće dogoditi i nekoliko anegdotalnih izvještaja o trudnoći unutar ispitivanja nisu dovoljan dokaz da to ne utječe na populacijsku razinu.
CJEPIVO COVID UZROKUJE POREMEĆAJE KRVI
Drugo, sve genske terapije (Covid cjepiva) uzrokuju koagulopatiju. (Koagulopatija – kada je oštećen sustav zgrušavanja krvi u tijelu.) To nije izolirano od jednog proizvođača. I ovo nije izolirano za jednu dobnu skupinu. Kao što vidimo smrt od koagulopatije kod zdravih mladih odraslih osoba bez sekundarnih popratnih bolesti. Od 9. travnja 2021. u sustavu izvještavanja VAERS zabilježeno je 795 izvještaja povezanih s poremećajima zgrušavanja krvi, od čega 338 zbog trombocitopenije.
Postoje naprijed i unatrag mehanicistički principi zašto se to događa. Poznato je da prirodna infekcija uzrokuje koagulopatiju zbog proteina klasja. Sva cjepiva za gensku terapiju usmjeravaju tijelo na stvaranje bjelančevina. Zhang i suradnici u (znanstvenom radu objavljenom u Journal of Hematology & Oncology) u rujnu 2020. godine pokazali su da ako ukapate protein klasova miševima koji su humanizirali ACE-2 receptore na trombocitima, dobit ćete i diseminiranu trombozu.
Protein šiljak inkubiran s ljudskom krvlju in vitro također je uzrokovao razvoj krvnih ugrušaka koji je bio otporan na fibrinolizu. (Fibrinoliza je tjelesni proces razgradnje krvnih ugrušaka). Protein spike uzrokuje trombocitne događaje, koji se ne mogu riješiti prirodnim putem. I sva cjepiva moraju biti zaustavljena u nadi da se mogu preoblikovati kako bi se zaštitila od ovog štetnog učinka.
POSTOJE SNAŽNI DOKAZI ZA IMUNOLOŠKI BIJEG
U ovom trenutku usmenog svjedočenja dr. Janci Chunn Lindsay prekinuo je muški glas: “Hvala na komentaru, vaše vrijeme je isteklo.” Posegnuo sam doktorici Janci Chunn Lindsay kako bih saznao što je još željela podijeliti s ACIP-om, uz njezinu zabrinutost zbog poremećaja plodnosti i zgrušavanja krvi. Poslala mi je natrag svoju treću točku, koju je predala kao pismeno svjedočenje.
Treće, postoje snažni dokazi za imunološki bijeg i da inokulacija pod pandemijskim pritiskom ovim procurivim cjepivima potiče stvaranje više smrtonosnih mutanata koji ujedno novo zaraze demografsku populaciju mlađe dobi i uzrokuju više smrtnih slučajeva povezanih s Covidom nego što bi to učinili su se dogodile bez intervencije. Odnosno, postoje dokazi da cjepiva pogoršavaju pandemiju.
Jasno je da vidimo privremenu imunološku depresiju odmah nakon cijepljenja (vidi World Meter Global Covid brojanje smrtnih slučajeva nakon datuma cijepljenja), a postoje imunosupresivna područja na bjelančevinama klasova, kao i Syn-2, koja bi to mogla vjerojatno uzrokovati, putem mehanizma posredovanog T-stanicama. Ako ne zaustavimo ovu kampanju cjepiva dok se ti problemi ne istraže, mogli bismo vidjeti fenomen kakav vidimo kod pilića s Marekovom bolešću.
Sad imamo dovoljno dokaza da vidimo jasnu korelaciju s povećanim brojem smrtnosti od Covida i kampanjama cjepiva. To nije slučajno. To je nesretan neželjeni učinak cjepiva. Jednostavno ne smijemo zatvarati oči i pretvarati se da se to ne događa. Moramo odmah zaustaviti cijelu primjenu cjepiva Covid, prije nego što stvorimo istinsku pandemiju u kojoj nećemo moći vladati.
Znanstvenica s MIT-a također je zabrinuta zbog zgrušavanja krvi i problema s plodnošću.
Stephanie Seneff, doktorica znanosti, stručnjakinja za sintezu proteina, vjeruje da je hipoteza dr. Lindsay točna. “Apsolutno dijelim ove zabrinutosti”, napisala mi je dr. Seneff, viši znanstveni istraživač s MIT-a, u e-pošti.
„Potencijal poremećaja zgrušavanja krvi i potencijal sterilizacije samo su dio priče. Postoje i drugi potencijalni dugoročni učinci ovih cjepiva, poput autoimune bolesti i imunološkog bijega, pri čemu cjepiva primijenjena na imunološki ugrožene ljude ubrzavaju stopu mutacije virusa tako da dovode do prirodno stečenih i cjepiva induciranih antitijela više nije na snazi.”
Poput dr. Lindsay, i dr. Seneff vjeruje da moramo odmah zaustaviti kampanje za Covid cjepiva. “Ovo masovno kliničko ispitivanje na općoj populaciji moglo bi imati razorne i nepovratne učinke na ogroman broj ljudi”, objašnjava Seneff.
Unatoč ovim problemima s plodnošću i poremećajima krvi, CDC-ov odbor prošli je petak izglasao nastavak primjene cjepiva Johnson i Johnson . Ipak su predložili da se doda oznaka upozorenja FDA-e. Njihov argument protiv zaustavljanja cijepljenja protiv Covida?
CDC vjeruje da su koristi veće od rizika! Luđe ne može biti! Na FB dr Slađane Velkov zanimljiva je objava oko izvješća Pfizer cjepiva i njegovih dugoročnih posljedica.
https://www.facebook.com/1301708254/posts/10225888277135865/
FAJZEROVA CJEPIVA POTVRĐENO IZAZIVAJU NEURODEGENERATIVNE BOLESTI
“U novom šokantnom izvještaju o cjepivima protiv COVID-19 otkriveno je da cjepivo protiv koronavirusa Pfizer može imati dugoročne zdravstvene posljedice, koje nisu prethodno otkrivene, uključujući ALS, Alzheimerovu bolest i druge neurološke degenerativne bolesti”.
“Aktuelna SARSCoV-2 cjepiva, zasnovane na RNA, odobrene su u SAD-u po hitnom postupku bez opsežnih dugoročnih sigurnosnih ispitivanja”, navodi se u izveštaju. “U ovom radu cjepivo Pfizer COVID-19, je evaluirana na potencijalnu mogućnost indukcije bolesti zasnovane na prionima kod primalaca cjepiva. “Prema CDC-u, bolesti na bazi priona oblik su neurodegenerativnih bolesti, što znači da Pfizer vakcina može potencijalno izazvati dugotrajnu štetu i negativne efekte na moždano tkivo.
To je posebno zabrinjavajuće jer je Pfizer mRNA cjepivo, neprovjerena vrsta cjepiva koja stvara nove proteine i koja se zapravo može integrirati u ljudski genom, navodi se u izveštaju Nacionalne medicinske biblioteke. Drugim riječima, degenerativna stanja mozga mogu se pojaviti u bilo kom trenutku vašeg života nakon primanja vakcine.
O tome smo pisali a Faktografić nas napao da širimo dezinformacije.
Evo nas, sve ide kroz službene izvještaje CDC-a. “RNA sekvenca vakcine, kao i ciljana interakcija spike proteina, analizirani su na potencijal pretvaranja unutarćelijskih RNA vezujućih proteina, TAR DNA vezujućih proteina (TDP-43) i stopljeni u sarkomu (FUS) u njihove patološke prionske konformacije”, objašnjava se u izvještaju.
TDP-43 je protein za koji je poznato da izaziva demenciju, ALS, pa čak i Alzheimerovu bolest, navodi Alzpedia. Slično tome, poznato je da protein FUS izaziva ALS i nasljedna esencijalna podrhtavanja, prema bazi podataka o humanom genomu.
Eksperiment izveden za potrebe izvještaja je bio da se utvrdi da li se ova dva štetna proteina ugrađuju u našu DNK, kao što se očekuje od mRNA cjepiva. Izveštaj je utvrdio da “RNA cjepiva imaju specifične sekvence koje mogu navesti TDP-43 i FUS da se preklope u svoje patološke potvrde o prionima”, što znači da se oba proteina mogu ugraditi u našu DNK i uzrokovati štetne neurološke bolesti.
Rezime izvještaja zaključuje da “Priloženi nalaz, kao i dodatni potencijalni rizici, navode autora da vjeruje da je regulatorno odobrenje cjepiva zasnovanih na RNA za SARS-CoV-2 preuranjeno i da cjepivo može nanijeti mnogo više štete nego koristi. “Sam izvještaj završava sa ovim upozorenjem: “Cjepiva bi mogla biti bio oružje i čak opasnije od izvorne infekcije.”
I o tome smo već pisali:
National File je zapravo kontaktirao CDC kako bi se raspitao zašto se Pfizer cjepiva i dalje distribuiraju usprkos ovim vjerodostojnim navodima. Prije objavljivanja nije primljen odgovor.”
https://scivisionpub.com/pdfs/covid19-rna-based-vaccines-and-the-risk-of-prion-disease-1503.pdf
https://nationalfile.com/report-pfizer-vaccine-confirmed-to-cause-neurodegenerative-diseases/
I America’s Frontline Doctors su se prošli tjedan oglasili o cjepivu.
Tako kažu da „oni koji su cijepljeni uzrokuju novu COVID pandemiju.“ Niste li se pitali, kako je moguće da COVID 19 virus nema sezonu, nije ovisan o geografskoj širini i ima famozne valove (prvi, drugi, treći itd…)
Odgovor na vaše pitanje mogao bi biti u najnovijem istraživanju Američkih Frontline doktora, koji su upozorili da cijepljene osobe mogu biti izvor širenja zaraze, te na taj način poticati i podržavati COVID pandemiju.
U svom najnovijem izdanju, američki Frontline doktori (AFLDS) upozorili su kako spike proteini koji nastaju u stanicama primatelja COVID-19 eksperimentalnih cjepiva, imaju sposobnost:
- Prolaziti kroz „krvno -moždanu barijeru ” i na taj način uzrokovati neurološka oštećenja
- Sa cijepljene osobe mogu se ”širiti” na druge osobe u njihovoj blizini, uzrokujući na taj način bolest kod necijepljene djece i odraslih.
Dokument objavljen prošlog tjedna pod naslovom ”Identificiranje komplikacija nakon cijepljenja i njihovi uzroci: analiza podataka o pacijentima Covid-19 “ (“Identification of complications after vaccination and their causes: analysis of Covid-19 patient data”), pruža dodatne informacije zabrinutim građanima, zdravstvenim stručnjacima i donositeljima političkih odluka o neželjenim događajima i drugim pitanjima koja se pojavljuju kod cijepljenih osoba.
Frontlines doktori istaknuli su tisuće štetnih događaja povezanih s eksperimentalnim COVID-19 „cjepivima“ koja su zabilježena od strane Centra za kontrolu i prevenciju bolesti (CDC) i u Sustavu izvještavanja o neželjenim događajima cjepiva (VAERS).
Promatrajući bliže ove podatke, Frontline doktori iznose “neke ključne činjenice koje zabrinjavaju javnost, a nisu do sada obrađene od strane glavnih administracija za lijekove.”
Prvo, postoje značajni strahovi u vezi sa širokom distribucijom ovih novih tzv. cjepiva, koja koriste novu tehnologiju i ostaju još uvijek samo eksperimentalna bez punog odobrenja FDA. Umjesto da koriste oslabljeni antigenski odgovor – kao što se to događa kod konvencionalnih cjepiva – ovi eksperimentalni agensi unose nešto što se naziva ” spike protein ” u nečiji sustav.
„Nitko definitivno ne zna dugoročne zdravstvene posljedice na tijelo i mozak, posebice među mladima, povezane s ovim spike proteinom. Uz to, ako se dokažu problemi, nikada neće biti načina da se preokrenu štetni učinci kod onih koji su već cijepljeni. “
Drugo, za razliku od konvencionalnih cjepiva, ovi spike proteini, zajedno s “lipidnim nanočesticama” koje su sastavni dio stabilizacije cjepiva, imaju sposobnost prolaska kroz ”krvno-moždanu barijeru ” koja služi upravo tome da zaštiti osjetljiva područja mozga od otrovnih supstanci.
“Jednostavno nije bilo dovoljno vremena da se sazna koji su to moždani problemi i koliko često bi oni mogli nastati nakon cjepiva “, upozorava dokument. Rizici od takvog prodora spike proteina u živce i mozak uključuju „kroničnu upalu i trombozu (zgrušavanje) u neurološkom sustavu, pridonoseći premoru, kroničnoj letargiji, moždanom udaru, Bellovoj paralizi i simptomima tipa ALS. Nanočestice lipida iz cjepiva mogu se potencijalno stopiti s moždanim stanicama, što rezultira odgođenom neurodegenerativnom bolešću.
M-RNA inducirani spike protein u cjepivima može se vezati za moždano tkivo 10 do 20 puta jače, od prirodnog spike proteina koji je nađen u samom virusu COVID-19.“ Budući da ova eksperimentalna tzv. cjepiva proizvode trilijune spike proteina u svojim primateljima, cijepljene osobe stoga “mogu izbaciti neke od tih čestica (spike proteina) prilikom bliskog kontakta s drugim osobama”, uzrokujući bolest i onima koji nisu cijepljeni.
A kako ludilo ide dalje evo i najnovijeg, naši stožeraši svojim odlukama i ucjenama krenuli su i na djecu, bez imalo ustezanja, bez bilo kakvih provjera, no na ovaj način pobit će nam svu mladost. Sve ove zločince koji ovo provode treba popisati, doći će uskoro vrijeme kad će i odgovarati.
*
*
*
*
https://www.logicno.com/politika/cijepi-li-se-ljude-eksperimentalnim-cjepivima.html
https://dokumentarac.hr/cijepljenje/cjepiva-ono-sto-ne-znamo/
*
Earlier this month, Pfizer became the first COVID vaccine maker in the U.S. to apply for full licensing from the U.S. Food and Drug Administration (FDA). In the wake of that announcement, Peter Doshi, senior editor of The BMJ, published an article questioning the wisdom of rushing the vaccine to full approval on the basis of only about six months’ worth of data.
Doshi pointed out that one key difference between the Emergency Use Authorization (EUA) granted by the FDA to Pfizer, Moderna and Johnson & Johnson COVID vaccines, and approval — also called “licensure,” or for vaccines, Biologics License Application (BLA) — was the expected length of follow-up of trial participants.
For EUA, the FDA requires two months follow-up of clinical trial participants, but the agency has not committed to a clear minimum follow-up requirement for full approval, Doshi said. When the question was raised during a Dec. 10, 2020, FDA meeting, Doshi reported that the FDA’s Doran Fink responded that the agency “typically asks” for “at least six months of follow-up in a substantial number of clinical trial participants to constitute a safety database that would support licensure.”
*
„Razboritost bi čak nalagala da se u svim zemljama kojima su ta cjepiva protiv COVIDA-19 (SARS-CoV-2) prodana, sve tako puštene serije odmah povuku; i da bi ovo uvjetno MA odobrenje trebalo hitno suspendirati ili čak otkazati do daljnjeg.“
Centre Territorial d’Information Pharmaceutique d’Avis (CTIAP za francuski akronim) zaključio je da niti jedno od četiri cjepiva koja se primjenjuju u Francuskoj nije sigurno ili učinkovito. Sva su dobila uvjetna odobrenja i to samo za hitnu uporabu s nedovoljnim kliničkim dokazima, zbog čega su zatražili njihovu trenutnu obustavu.
CTIAP, koji je povezan s javnom bolnicom Cholet u zapadnoj Francuskoj, nedavno je objavio izvješće koje pokazuje da cjepiva koja se koriste protiv C0VIDA-19 nisu podvrgnuta kliničkim ispitivanjima. Također, nedostaje evaluirana kvaliteta: aktivnih tvari, njihovih “pomoćnih tvari – od kojih su neke nove” i proizvodnih postupaka.
https://ctiapchcholet.blogspot.com/2021/04/inedit-exclusif-vaccins-contre-la-covid.html
Doktorica Catherine Frade koja vodi istraživački tim, poznata je farmaceutkinja koja je radila na javnim podacima objavljenim u izvješću Europske agencije za lijekove (EMA) u vezi s injekcijama Pfizer, Moderne, AstraZenece i Janssena (Johnson & Johnson).
Prvo upozorenje objavljeno u izvješću je da svi ti proizvodi imaju samo uvjetna odobrenja za puštanje u promet (MA). Osim toga, svi su oni predmet daljnjih istraživanja do 2024. godine, što ih čini gotovo nemogućim za dovršiti s obzirom na ubrzani način distribucije cjepiva.
S tim u vezi, CTIAP upozorava da su se sva ta cjepiva počela stavljati u promet i aktivno primjenjivati na ljudima prije nego što su se provela „ispitivanja kvalitete aktivne tvari i gotovog proizvoda”: Svi proizvodni laboratoriji imaju buduće rokove za podnošenje studija u vezi s tim. Iako znaju da će do trenutka kada ih predaju, mnogi stanovnici svijeta već biti cijepljeni.
Izvještaj ne ukazuje na to da su cjepiva opasna, ali trenutačna saznanja nisu dovoljno valjana da bi se pokazala njihova učinkovitost i / ili sigurnost.
Cjepiva su se počela proizvoditi i primjenjivati usred laboratorijskih ispitivanja, što podrazumijeva da bi promjena rezultata tijekom sljedećih nekoliko mjeseci mogla onesposobiti bilo koja prethodna ispitivanja, jer su još uvijek u razdoblju istraživanja i prilagodbe.
Izvještaj povlači zanimljivu paralelu između proizvodnje cjepiva i proizvodnje automobila. Pita se da li bismo zamislili da je moguće pokrenuti proizvodnu liniju za novi automobil i započeti ga s plasiranjem bez dovršavanja studija kvalitete svakog od njegovih dijelova i motora, uključujući sigurnosne komponente poput njegovih kočnica i električnih sustava.
Logičan je odgovor NE, pa zašto bismo to činili s cjepivima, tvari namijenjenima da se izravno ubrizgavaju u tijelo svakog čovjeka na svijetu?
Izvještaj zaključuje: „Razboritost bi čak nalagala da se u svim zemljama kojima su ta cjepiva protiv COVIDA-19 (SARS-CoV-2) prodana, sve tako puštene serije odmah povuku; i da bi ovo MA odobrenje trebalo hitno suspendirati ili čak otkazati do daljnjeg.“
Izvor: https://thebl.tv/politics/french-drug-evaluation-center-concludes-all-4-covid-vaccines-should-be-discontinued.html
https://ctiapchcholet.blogspot.com/2021/04/inedit-exclusif-vaccins-contre-la-covid.html
*
*
The team led by Dr. Catherine Frade, a pharmacist, worked on public data released by the EMA with relation to the Pfizer, Moderna, AstraZeneca and Janssen (Johnson & Johnson) shots, and its first caveat was that all these products only have temporary marketing authorizations. They are all subject to further studies that reach as far as 2024 and even beyond, and these will be almost impossible to be completed because of the way the vaccines are now being distributed, said the CTIAP report.
These studies even include the stability and comparability of the vaccine batches put on the market and the quality and safety of excipients — substances formulated alongside the active ingredient of a medication to facilitate or enhance their absorption.
No proof of quality
According to the CTIAP, all of the vaccines were put on the market and actively used on human beings before “proof of quality for the active substance and the finished product” was produced: all the manufacturing labs obtained future deadlines to submit their studies in this regard.
The authors of the report consider that the “variabilities, which impact the very core of the product, could even invalidate any clinical trials conducted” in the coming months and years.
They go so far as to state: “Prudence would even dictate that, in all countries where these vaccines against COVID-19 have been marketed, all the batches thus ‘released’ should be withdrawn immediately; and that these MAs that have been granted should be suspended, or even canceled, as a matter of urgency until further notice.”
LifeSite’s translation of the CTIAP’s April 2 report
Can we imagine launching a car manufacturing line and putting vehicles on the road, despite the uncertainties noted in the official documents published? These uncertainties are related to the quality of the parts making up the engine and the various other parts, including those related to safety, the manufacturing process, the reproducibility of the batches that are being marketed, etc.
In the field of medicines (including vaccines), the pharmaceutical act of “release” of the finished product (an authorized product intended for sale) constitutes the final stage of control that precedes the release of these products to the population. This key step of “release” is under the pharmaceutical responsibility of the manufacturers.
Following its previous analyses, the CTIAP of the Cholet Hospital Center has once again revealed to the public, and probably in an unprecedented and exclusive way, new vital information concerning the following four vaccines against COVID-19: the one from the BioNTech/Pfizer laboratory; the one from the Moderna laboratory; the one from the Astra Zeneca laboratory; the one from the Janssen laboratory.
This work was made possible thanks to the valuable contribution of Dr. Catherine Frade, pharmacist and former director of international regulatory affairs in the pharmaceutical industry. She graciously provided us with a documented, written alert. Read here.
In this document, she sheds light on data extracted, on March 22, 2021, from the MA (marketing authorization) itself; an MA qualified as “conditional.” She has extracted “source data that is difficult to identify by someone who does not work in the field.” This data is therefore public and verifiable. First of all, it should be noted that the author of this document no longer works in the pharmaceutical industry; she states: “First of all, I would like to make it clear that I have no conflict of interest with the pharmaceutical industry.” It is therefore with her agreement that CTIAP intends to make available to the public, health professionals, decision-makers … an analysis of some of these data that all should read carefully.
This reflection first presents what a “conditional” MA is (I). Then, it recalls that the studies for these vaccines are not complete, as they run from “2021 to at least 2024” (II). Then, it reveals, in an unprecedented and exclusive way, that the official documents, published by the European Medicines Agency (EMA), underline the insufficiency of the evidence concerning also the “quality” of the “active substance” and of the “excipients,” of the “manufacturing process,” of the “reproducibility of the batches” that are being commercialized, etc. (III). Finally, this analysis proposes a conclusion.
Analysis Conclusion
I — We must to understand what a “conditional” MA is
An MA is to a drug what a car registration document is to a car. MA is granted when a drug has proven its quality, efficacy, and safety; with a positive benefit/risk ratio: that is, it presents more benefits than risks. Obtaining this MA is the essential condition for a pharmaceutical laboratory to sell any drug, including vaccines.
Here, in the case of these vaccines against COVID-19, the four MAs issued are so-called “conditional” MAs. They are temporary. They are valid for no more than one year, because they were obtained on the basis of “incomplete data.” To obtain a standard 5-year MA, the laboratories concerned must provide dossiers completed with “studies in progress and studies planned for the coming years.” Throughout “this development,” close and coordinated monitoring between the manufacturing laboratories and the health authorities is organized through regular discussions. The “conditional” MA is “re-evaluated each year” according to the contribution and critical analysis of additional data provided and collected during a full year.
This “conditional” MA is a European MA. It was obtained through the centralized accelerated procedure. It allows simultaneous marketing in the following 30 countries (European Union and European Free Trade Association): Austria, Belgium, Bulgaria, Croatia, Cyprus, Czech Republic, Denmark, Estonia, Finland, France, Germany, Greece, Hungary, Iceland, Ireland, Italy, Latvia, Liechtenstein, Lithuania, Luxembourg, Malta, Netherlands, Norway, Poland, Portugal, Romania, Slovakia, Slovenia, Spain, Sweden.
The studies concerning these four vaccines are therefore still in progress.
II — The planned studies are still in progress and are spread over a period ranging from “2021 to at least 2024”
All of the studies submitted during the MA application are summarized in the EPAR (European Public Assessment Report). This report is published on the European Medicines Agency (EMA) website. The planned studies, not yet completed, are also included.
This schedule, which “extends from 2021 to at least 2024,” depending on which COVID-19 vaccine is involved, is defined in the “annexes” of the conditional marketing authorization and in the published EPARs.
As an example, the BioNTech/Pfizer vaccine received this European conditional MA on December 21, 2020. And the deadline for filing “confirmation” of efficacy, safety, and tolerability of this vaccine is “December 2023.”
The Moderna vaccine was granted marketing authorization on January 6, 2021. The deadline for filing “confirmation” of efficacy, safety, and tolerability of the vaccine is “December 2022” at the earliest.
AstraZeneca’s vaccine was granted marketing authorization on January 29, 2021. The deadline for filing “confirmation” of efficacy, safety, and tolerability of the vaccine is “March 2024.”
The Janssen vaccine was granted conditional European marketing authorization on March 11, 2021. The deadline for submitting “confirmation” of the vaccine’s efficacy, safety and tolerance is “December 2023.”
However, to date — and this is undoubtedly where the unprecedented and exclusive revelation of this study lies — another deadline has been set for these four vaccines. This deadline no longer concerns only the ongoing clinical trials, but also the “proof of quality for the active substance and the finished product” itself: that is, the intrinsic quality (the heart) of the product sold and administered to millions of people.
III — The published official documents also underline the incompleteness of the evidence concerning the “quality” of the “active substance” and “excipients,” the “manufacturing process,” the ”reproducibility of the batches marketed”, etc.
The deadline for submitting additional evidence on the “quality” of the “active substance” and the “finished product” (i.e., the vaccine that is authorized and sold) is set for:
- “July 2021” for BioNTech/Pfizer;
- “June 2021” for Moderna;
- “June 2022” for Astra Zeneca;
- “August 2021” for Janssen.
Indeed, for these 4 vaccines, paragraph E, “Specific obligation regarding post-authorization measures for the conditional marketing authorization,” taken from Annex II of the MA, clearly states the following:
For the BioNTech/Pfizer vaccine (pages 18-19)
By “March 2021,” the laboratory must provide “additional validation data” to “confirm the reproducibility of the finished product manufacturing process.”
By “July 2021,” the laboratory must provide missing information to:
-
- “complete the characterization of the active substance and the finished product;”
- “strengthen the control strategy, including the specifications of the active substance and the finished product” in order to “ensure the constant quality of the product;”
- “provide additional information regarding its synthesis process and control strategy” in order to “confirm the purity profile of the excipient ALC-0315” and “to ensure quality control and batch-to-batch reproducibility throughout the life cycle of the finished product;”
- and by “December 2023,” and “in order to confirm the efficacy and safety” of this vaccine, the company “shall submit the final clinical study report for the randomized, placebo-controlled, blind observer study (Study C4591001).
For the Moderna vaccine (page 15)
The laboratory should provide the missing information to:
-
- “complete the characterization of the manufacturing processes of the active substance and the finished product” (deadline “January 2021”);
- confirm the reproducibility of the manufacturing process of the active substance and the finished product (initial and final batch sizes) (deadline “April 2021”);
- “provide additional information on the stability of the active substance and the finished product and review the specifications of the active substance and the finished product after longer industrial practice” with the aim of “ensuring consistent product quality” (deadline “June 2021”);
- “submit the final study report for the randomized, placebo-controlled, blinded clinical trial for the mRNA-1273-P301 observer” to “confirm the efficacy and safety of COVID-19 vaccine Moderna” (by December 2022).
For the Astra Zeneca vaccine (pages 14-15)
The laboratory must submit the missing information in order to:
-
- “provide additional validation and comparability data, and initiate further testing” with the aim of “confirming the reproducibility of the manufacturing processes of the active substance and the finished product” (by “December 2021”);
- “Provide the main analysis (based on the December 7 data cut-off (post database lock) and the final analysis of the combined pivotal studies” to “confirm the efficacy and safety of COVID-19 Vaccine AstraZeneca” (deadline “March 5, 2021” (for the main analysis) and “May 31, 2022” (for the combined analysis);
- “submit final reports of the randomized controlled clinical studies COV001, COV002, COV003 and COV005” to “confirm the efficacy and safety of COVID-19 Vaccine AstraZeneca” (due “May 31, 2022”);
- “provide additional data regarding the stability of the active substance and the finished product and revise the specifications of the finished product after extensive industrial practice” in order to “ensure consistent product quality” (deadline “June 2022”);
- “submit the synthesis and summaries of the primary analysis and the final clinical study report for study D8110C00001” to “confirm the efficacy and safety of COVID-19 vaccine AstraZeneca in the elderly and in subjects with underlying disease” — due “April 30, 2021” (for the primary analysis) and “March 31, 2024” (for the final study report).
For the Janssen vaccine (page 18)
The laboratory should submit the missing information to:
-
- “provide additional comparability and validation data” to “confirm the reproducibility of the manufacturing process of the finished product” (deadline “August 15, 2021”);
- submit the final report of the VAC31518COV3001 randomized, placebo-controlled, single-blind clinical study to “confirm the efficacy and safety of the COVID-19 Ad26.COV2.S vaccine” by December 31, 2023.
These facts allow us to offer a conclusion.
EMA Conclusion
For these reasons, which are not exhaustive, it has proved useful to look for and read the content of the paragraph E: “Specific obligation relating to post-authorization measures concerning the conditional marketing authorization,” extracted from Annex II of the MA, corresponding to each of these 4 vaccines against COVID-19.
The inadequacy of the evaluation does not only concern the clinical trials (studies conducted in humans (women and men)), but also the quality of the active substance, the excipients (some of which are new) the manufacturing process, and the batches released and administered to humans in several countries around the world.
Moreover, these new excipients must be considered as new active ingredients, and thus be the subject of a complete evaluation file similar to that required for a new active ingredient.
Changing the commercial name of one of these vaccines, as was recently announced for the AstraZeneca vaccine in particular, can only be considered as a cosmetic arrangement of the product’s image for marketing purposes (winning new public confidence, boosting sales). It would not answer the questions raised concerning the quality, efficacy and safety of the product. This is one of the usual techniques used to put make-up on (dissimulate) certain undesirable characteristics of the product concerned. It is a technique that has been used to present other drugs in the best possible light.
As already mentioned, in the field of medicines (including vaccines), the “release” of the finished product (intended for sale) is the final stage of control (of quality and therefore of safety) before making these products available to the population.
This key stage of “release” of batches is the pharmaceutical responsibility of the manufacturers. However, the responsibility of the users (institutions and health professionals in particular) may also be involved.
In our opinion, these clinical studies should never have begun before the intrinsic quality of the finished product and its manufacturing process had been fully mastered; before the formulas of these vaccines had been stabilized.
How can the results of these clinical trials, conducted on a global scale, be compared if the vaccine administered can vary from one manufacture to another, from one batch to another, from one region to another?
These variabilities, which impact the very core of the product, could even invalidate any clinical trials conducted.
Even in the case of a health emergency, it is therefore difficult for us to understand the basis for the MA (marketing authorization) that has been granted to these COVID-19 vaccines.
In addition to the uncertainties related to COVID-19, there are also the approximations related to the use, and the intrinsic quality, of these vaccines. Now two problems will have to be managed instead of one.
The maneuver seems subtle. The useful information is available in the official documents published in the framework of the MA; but this data is not made visible by the official discourse. It seems the latter has only tried to present these products as being effective and safe, without reservations; even though the formulas and manufacturing processes of these vaccines do not even seem to have been fully stabilized yet.
These new revelations, which are undoubtedly unprecedented and exclusive, further cast doubt on the validity of consent (a fundamental freedom) that is supposed to be free and informed, and which is said to have been given by the people who are now already vaccinated.
Every person has the right to clear, fair and appropriate information. This information is also perennial: if new data is revealed, those already vaccinated must be informed a posteriori (after the administration of this or that vaccine).
The “obligation” to vaccinate cannot therefore be sustained, even in a disguised form, notably through a “vaccine passport.”
This new analysis further confirms our previous reflections such as the one entitled “Could the Covid-19 vaccine (Tozinameran; COMIRNATY°) be qualified as ‘defective’ by a judge?”. Read here.
Or those expressed in the two open letters that have already been sent to the Minister of Solidarity and Health and to the seven Orders of health professionals.
https://int.artloft.co/why-did-a-french-drug-assessment-center-demand-removal-of-all-four-widely-used-covid-vaccines/
*
Ali bi lahko sodnik cepivo proti Covid-19 (Tozinaméran; COMIRNATY °) označil za "okvarjeno"?
» Učinkovitost cepiva bo najprej odvisna od naše sposobnosti krepitve zaupanja . Odgovoriti na vprašanja, odpraviti dvome, zmanjšati strahove, na to se moramo osredotočiti v prihodnjih tednih. Na vseh ozemljih v vsaki občini so zdravniki in zdravstveni delavci mejnik, spoštovana osebnost, katere glas poslušajo in slišijo. Tesni odnosi, ki vas vežejo na naše sodržavljane, so edinstveni. " (Minister za solidarnost in zdravje; v " PORTFOLIO ", priloženem " Vodniku po cepljenju za zdravnike, medicinske sestre in farmacevte ", objavljenem 31. decembra 2020)
Ne, učinkovitost cepiva je najprej odvisna od podatkov, potrjenih v kliničnih preskušanjih (izvedenih pri ljudeh). Vloga zdravstvenega delavca je predvsem zagotavljanje jasnih, poštenih in ustreznih informacij za pridobitev prostega in informiranega soglasja osebe; kot mu nalagajo zlasti kodeks javnega zdravja in pravila njegovega reguliranega poklica.
Zdi se, da nas upravljanje Covid-19, povezano s Sars-CoV-2, popelje v obdobje post-znanosti in post-prava. Primer cepiva proti Covid-19 bi lahko ponazoril to ugotovitev.
Ta razmislek vam ponuja razmišljanje v treh stopnjah, kot bi to storil sodnik: prvič, slednji opredeljuje pravno državo (I) ; nato to pravilo sooči z dejstvi subjekta (vrste: tukaj cepivo proti Covid-19) (II) ; in nazadnje naredi zaključek (reši spor) (III) .
I- Kaj je po zakonu "okvarjen" izdelek?
Cepivo je zdravilo. Je "izdelek" v smislu civilnega zakonika.
Na splošno se v primeru škode zaradi neželenih učinkov, za katere se domneva, da so medicinskega izvora, sodnik zlasti opira na nekatere določbe tega civilnega zakonika, da prevzame odgovornost proizvajalca (farmacevtskega laboratorija) tega "okvarjenega" izdelka .
Žrtev mora dokazati številne elemente, vključno z "napako" izdelka. Po civilnem zakoniku je izdelek okvarjen, če "ne ponuja varnosti, ki bi jo lahko upravičeno pričakovali" . Nevarnost izdelka je lahko na različnih ravneh: oblikovanje, izdelava, uporaba itd. Sodnik upošteva nekatera merila, kot so predstavitev izdelka, uporaba, za katero je namenjen itd.
Več sodnih odločb (sodna praksa) posebno pozornost namenja navodilom, ki so priložena izdelku. Nezadostne informacije o tveganjih zdravila (cepiva) omogočajo sodniku, da ugotovi omenjeno napako tega zdravila. Tudi če je tveganje omenjeno v tem navodilu, se lahko odgovornost proizvajalca obdrži zlasti, če zdravilo predstavlja neugodno razmerje med koristjo in tveganjem (tveganje je večje od koristi).
Na posebnem področju cepiv in od leta 2008 se zdi, da je najvišja sodna pristojnost (kasacijsko sodišče) svojo sodno prakso premaknila v smer, ki je ugodnejša za žrtev: napako je mogoče dokazati s preprosto domnevo, če temelji o "resnih, natančnih in skladnih indeksih"na primer časovna bližina med injiciranjem cepiva in pojavom neželenih učinkov; odsotnost osebne in družinske anamneze v zvezi s temi stranskimi učinki; obstoj znatnega števila opisanih in objavljenih primerov, ki poročajo o teh škodljivih učinkih po dajanju omenjenega cepiva ... Sodišče Evropske unije (Sodišče Evropskih skupnosti) je leta 2017 to možno uporabo dokazov potrdilo z domnevo. Laboratorij lahko predloži nasprotni dokaz. Kljub temu dogajanju je položaj sodnikov še negotov. Žrtev je lahko razočarana.
II- Uporaba te pravne države za cepiva proti Covid-19
V tem primeru se je treba zlasti na primeru cepiva iz laboratorijev Pfizer / BioNTech (Tozinaméran; COMIRNATY °) vprašati, ali bi sodnik lahko ocenil , da je ta izdelek "okvarjen" . Isto vprašanje in enaka utemeljitev veljata tudi za druga cepiva proti Covid-19. Ta analiza je omejena na primer cepiva (Tozinaméran; COMIRNATY °), ki je prvi koristil „pogojno“ dovoljenje za promet (MA), zlasti v Franciji; in za katere imamo zato daljše spremljanje (v primerjavi z drugimi cepivi).
II.1- Regulator promovira urnik cepljenja, ki se razlikuje od urnika cepljenja, ki ga odobri dovoljenje za promet
7. januarja 2021, je varnostna agencija nacionalni drog (ANSM), sam, ki se zavzema za off-label uporabi tega cepiva. Dejansko je v svojem " mnenja (...) v zvezi z drugim odmerkom cepiva Comirnaty od Pfizer-BioNtech - informacijske točke" je ANSM meni, da je "rok za upravljanje 2 nd mogoče predvideti odmerek med 21 in 42 dni «Ob tem, da spomnimo, da je to cepivo » odobreno v Evropi « za » urnik dajanja «, ki » temelji na dveh odmerkih, ki sta v razmiku najmanj 21 dni «. Regulatorni organ, žandar za zdravila, si zato dovoljuje, da spremeni urnik cepljenja (odmerek zdravila), kot ga je odobrilo dovoljenje za promet. Zdi se, da tak odstop od MA potrjuje proizvajalec sam. Farmacevtsko podjetje se zato zdi previdnejše od regulatorja: laboratorijska datoteka Pfizer / BioNTech kaže na okrepitev 21 dni po prvi injekciji. ANSM je sledil nasvetom Evropske agencije za zdravila. Slednji opozarja, da je za takšen premik odgovoren predpisovalec. WHO (Svetovna zdravstvena organizacija) odobri ta premor.
Vendar pa je še več. Na področju, je v pojasnilu z dne 8. januar 2021 in razpošilja vse osebje, bolnišnica center ponuja svoj urnik cepljenja: uporaba dveh odmerkov razporejene na vsaj 19 dni narazen " . 5. januarja 2021 je po objavljenem cepljenju profesorja medicine, vodje oddelka v univerzitetnem bolnišničnem centru (CHU), tisk zapisal: "Vodja oddelka bo v desetih dneh prejel še eno injekcijo, tako da bo imunizacija skupaj " .
Drugi regulatorji, druge države, spoštujejo MA
Nemčija noče iti izven okvira MA in se je odločila, da ne bo odložila dajanja druge injekcije.
Ameriški regulativni organ (FDA: uprava za hrano in zdravila) meni, da ta uporaba, ki ni označena, ne temelji na nobenih razpoložljivih in zanesljivih podatkih.
Neznane posledice: možna tveganja
Taka sprememba urnika cepljenj otežuje odgovor na postavljena vprašanja: kakšna zaščita med obema injekcijama? Kako dober je imunski odziv po drugem odmerku?
Možna tveganja so lahko naslednja: bolezen, ki se poslabša s cepljenjem, avtoimunski stranski učinki, razvoj odpornosti virusa (Sars-CoV-2) na cepivo itd.
II.2- Vzorec s 6- th odmerek pa se vsebino čaše potrjene 5 odmerkov na NMA
Zdi se, da je bila promovirana še ena svoboda. Nekateri priporočajo cepljenje 6 oseb z vialo, ki je po podatkih dovoljenja za promet z zdravilom namenjena cepljenju 5 oseb. Vendar pa je preostala količina (kot bi nekateri uporabljajo za omenjene 6 th odmerek) omogoča zbiranje, natančno, je 5 rednih odmerkih in še posebej zadnje (5 th ) odmerek. Ta preostali volumen omogoča izpiranje igle in odstranitev zračnih mehurčkov iz brizge.
II.3- Vprašljivi, nepopolni ali celo netočni podatki, razširjeni prek dokumentov, ki so jih pripravili začasni organi
Napake
Na primer glede načina dajanja cepiva po intramuskularni (IM) poti je "PORTFOLIO", priložen " Vodniku po cepljenju za zdravnike, medicinske sestre in farmacevte" , objavljen 31. decembra 2020 na spletni strani ministrstva solidarnosti in zdravja, označuje: " Naredite kožno gubo med palcem in kazalcem" .
Toda v svoji različici z dne 5. januarja 2021 ta "PORTFOLIO" vsebuje popravek tega navodila: "Močno raztegnite kožo med kazalcem in palcem, ne da bi naredili kožno gubo " .
Na dan 31. decembra 2020 je ta dokument vseboval 61 strani. 5. januarja 2021 vsebuje le 26 strani.
Vprašljivi podatki o učinkovitosti cepiva
Na primer, v "listu 2 INFORMACIJE ZA REZIDENTE V OBSTAVIH ZA STAREJŠE IN NJIHOVE DRUŽINE" navedenega "PORTFOLIO" je navedeno naslednje:
"1. Zakaj se cepiti proti COVID-19? : Cepljenje proti COVID-19 vas bo zaščitilo pred zapleti in pojavom hudih oblik te bolezni. Študije so pokazale, da je cepivo zelo učinkovito pri zaščiti pred okužbami. "
V resnici pa je CTIAP, tako kot neodvisni pregled Prescrire , opazil "negotovost" glede učinkovitosti tega cepiva na omenjene "resne" oblike Covid-19 (glej članek z dne 26. decembra 2020).
Kot je prikazano v poročilu z dne 7. decembra 2020 o sestanku, ki ga je vodil delegat minister, pristojen za avtonomijo, je takšna učinkovitost predstavljena v obliki hipoteze, ki jo je treba dokazati: "to cepivo za permett bi močno zmanjšalo nevarnost resne oblike zaradi okužbe s COVID19 " . Besede imajo pomen; konjugacija glagola ima pomen: uporaba pogojnika je oblika previdnosti. To poročilo je bilo omenjeno med konferenco CTIAP 17. decembra 2020.
Ameriški regulativni organ (FDA: hrana in zdravila) je ugotovil, da rezultati kliničnih študij ne izpolnjujejo meril uspešnosti, ki so bili predhodno opredeljeni za hude oblike.
Avtorji v nasprotju trditvi so pozvane, da predložijo dokazilo o učinkovitosti cepiva, ki dokazuje, da znižanje v bolnišnico , od posledic do bolj ali manj dolgoročno, del življenjsko nevarne (bivanje v intenzivni) od smrti ... In prenos virusa ...
Nepopolni podatki o neželenih učinkih
Na primer, v tem istem "listu 2 INFORMACIJE ZA REZIDENTE V OBSTAVIH ZA STAREJŠE IN NJIHOVE DRUŽINE" je navedeno naslednje:
"4. Ali obstajajo kakšni stranski učinki tega cepljenja? Kot pri vseh cepivih se lahko po cepljenju pojavijo neželeni učinki: bolečina na mestu injiciranja, utrujenost, glavobol, bolečine v mišicah ali sklepih, nekaj mrzlice in rahlo zvišana telesna temperatura. Te motnje hitro izginejo. "
V resnici je ta seznam nepopoln, kar dokazujejo zlasti naslednji dokumenti:
Na spletni strani ANSM sta na voljo dva dokumenta
Povzetek glavnih značilnosti zdravila ( SPC ) in navodilo za uporabo, izdelano v okviru dovoljenja za promet z zdravilom (prim. Datoteke PDF, ki so na voljo v prikazani tabeli );
List "Neželeni učinki cepiva Pfizer / BioNTech COMIRNATY °: kaj morate vedeti" (na dnu strani, za isto tabelo).
Sporočilo za javnost Haute Autorité de Santé (HAS) z dne 24. decembra 2020 : kliknite tukaj
Članek v reviji Prescrire z dne 23. decembra 2020 : kliknite tukaj
Konferenca CTIAP 17. decembra 2020 : kliknite tukaj
Kodeks javnega zdravja in sodna praksa zahtevata informacije o pogostih ali resnih, celo izjemnih, neželenih učinkih .
II.4- Farmakovigilanca zaradi premajhnega obveščanja, ovir in nekaznovanosti
Na primer, in še vedno v istem "listu 2 INFORMACIJE ZA REZIDENTE V OBSTAVIH ZA STAREJŠE IN NJIHOVE DRUŽINE" je navedeno naslednje:
"V okviru nacionalne kampanje cepljenja proti COVID-19 Nacionalna agencija za varnost zdravil (ANSM) vzpostavlja poseben sistem za okrepljeno spremljanje škodljivih učinkov cepiv proti Covid-19 na francoskem ozemlju. "
8. januarja 2021 je ANSM objavil " Posodobitev stanja o nadzoru cepiv proti COVID-19", v kateri je zlasti navedeno, da "v tem drugem tednu cepljenja v Franciji niso opazili resnih škodljivih učinkov" .
Premajhna deklaracija
V resnici bi lahko zlasti v Franciji - ne da bi si nasprotovali - rekli, da so bili vsi možni resni škodljivi učinki izčrpno prijavljeni (prijavljeni) 31 regionalnim centrom za farmakovigilanco (CRPV), ki so razpršeni po celotnem območju. nacionalno ozemlje?
Ovire
Iz izkušenj lahko trdimo, da farmakovigilanca trpi zaradi premajhnega poročanja. Še huje, ugotovljene so ovire pri izjavi (glej članek CTIAP z dne 21. septembra 2019 z naslovom "PRAVICA ODZIVA NA OUEST-FRANCIJA." Upravni prepir "o zdravstveni budnosti. Nadaljevanje" Ovire za farmakovigilanco ": naše opozorilo je posredoval ANSM " ) .
"Organizirana nekaznovanost"
Poleg tega je v začetku julija 2018 neodvisni pregled Prescrire objavil članek z naslovom »Farmacevtska podjetja: organizirana nekaznovanost« . Ta članek nas obvešča, da je "inšpekcijski pregled, opravljen leta 2012", pokazal, da podjetje "ni analiziralo ali posredovalo agencijam za zdravila več kot 80.000 primerov suma škodljivih učinkov na 19 zdravil" . Za ko je sprejela "ponižno in skesano odnos" , je podjetje "iskanih uspešno" pridobitev "o prizanesljivosti evropskih organov" . Pregon se zato "ustavi" . Podjetje"Ne bo treba plačati skoraj 700 milijonov dolarjev globe . "
Tiskanje je razkrilo signale škodljivih učinkov v tujini, ki še niso potrjeni
Zdi se, da teh domnevnih škodljivih učinkov ni prenašal ves francoski tisk.
Glej članek z dne 6. januarja 2021 (točka "IV-C").
II.5- Druge negotovosti glede razmerja med koristjo in tveganjem
Podatki, ki jih lahko štejemo za relativno zadostne, se nanašajo na ljudi, stare od 18 do 75 let, učinkovitost pri blagih do zmernih oblikah, pa tudi na profil kratkotrajnih neželenih učinkov.
Vendar pa se MA izda od starosti 16 let.
Cepljenje se začne pri ljudeh, starejših od 75 let, ki so bili med kliničnimi preskušanji (pri ljudeh) slabo zastopani.
Prav tako razmerje med koristjo in tveganjem tega cepiva pri nosečnicah ni znano. Vendar se zdi, da pozornost mladih žensk v rodni dobi ni dovolj pritegnjena: vprašanje kontracepcije ni obravnavano.
Negotovosti zadevajo tudi doječe ženske, imunsko oslabljene, ljudi, ki so že imeli Covid-19, ljudi z rakom, ljudi z odpovedjo ledvic.
Razmerje med koristjo in tveganjem ni znano v primeru mutacij Sars-CoV-2.
Učinkovitost tega cepiva pri prenosu virusa še ni znana. Zaenkrat je treba še naprej spoštovati zlasti kretnje pregrade.
Učinkovitost in tveganja na srednji in dolgi rok niso znana. Zdi se, da bi bil tekoči projekt namenjen cepljenju ljudi v skupini, ki je prejemala placebo; zaradi česar bi bila analiza podatkov vsaj otežena: primerjava učinkovitosti in škodljivih učinkov med cepljeno skupino in kontrolno skupino (placebo) bo zapletena ali celo nemogoča.
(Za podrobnejšo analizo glej zlasti konferenco 17. decembra 2020).
Vmesni zaključek (iz poglavja "II")
Taka motnja je v nasprotju z besedami ministra za solidarnost in zdravje, ki to podpira v "PORTFOLIO" : "Če bodo zdravstveni delavci poklicani, da prevzamejo vodilno vlogo v kampanji cepljenja, ne bodo prepuščeni sami sebi. Dolžni smo vam, dolgujem vam jasne informacije in absolutno preglednost. To je namen dokumentov, ki so vam jih poslali. "
Opomba: cepivo in "zvezdniki" (zlasti s televizije)
Zaradi pomanjkanja zadostnih in preverljivih dokazov o odprtih vprašanjih v zvezi z razmerjem med koristjo in tveganjem tega cepiva ukrepajo medicinski, farmacevtski, novinarski, politični »zvezdniki« . Počutili bi se vloženi v civilizacijsko poslanstvo do sodržavljanov (preostalega prebivalstva, ki šteje več milijonov ljudi), ki bi bili nevedni.
Pred kamerami so "dali zgled", pravijo.
Bi vzeli ljudi za "otroke" ?
Zdi se, da nista razumela, da "slavnih" ne smemo zamenjati z razvpitostjo.
Zdi se, da vedno prezrejo, da "slavna oseba" ni del meril za ocenjevanje razmerja med koristjo in tveganjem zdravila (cepiva).
Kakšen žalosten "spektakel" ...
In na srečo gledalcev, da je omenjeno cepivo v obliki injekcije; in ne v rektalni obliki (pršilo, svečke itd.) ...
III- Sklep
Zaradi teh neizčrpnih razlogov, navedenih zgoraj, bi lahko to cepivo, vsaj uporabo tega zdravila in razširjenih informacij o njegovem razmerju med koristjo in tveganjem, civilno sodišče opredelilo kot "pomanjkljivo" . .
Kar zadeva kazensko odgovornost, bi to že močno vplivalo zlasti na zdravstvene delavce, za katere se zdi, da igrajo vlogo pri podpori nekaterih govorov, ki javno spodbujajo neuravnotežene, zavajajoče informacije, ki so v nasprotju s podatki, ki jih je pridobila znanost. Nekateri si celo upajo odkrito zagovarjati odpravo korakov, potrebnih za pridobitev privolitve (temeljna svoboda, zaščitena z notranjim in zunanjim pravom). Drugi si celo upajo žaliti ljudi, ki se upravičeno sprašujejo o razmerju med koristjo in tveganjem tega novega cepiva; in čeprav je samo MA "Pogojno" : to pomeni, da se ta MA za eno leto podeli zdravilu (cepivu), katerega razmerje med koristjo in tveganjem je premalo znano in ki ga je treba potrditi s pripravo dodatnih študij.
Poleg tega je v "listu: FOKUSIRANJE ODGOVORNOSTI" omenjenega "PORTFOLIO", ki ga je ustanovilo Ministrstvo za solidarnost in zdravje, jasno opozorjeno, da je "popolno nadomestilo zdravstvenih nesreč, ki jih je mogoče pripisati negovalnim dejavnostim, ki se izvajajo ob kampanjo cepiva proti covid-19 bo v okviru nacionalne solidarnosti zagotovil ONIAM [Nacionalni urad za odškodnine za zdravstvene nesreče] (...) Ta podpora nacionalne solidarnosti pa zdravstvenih delavcev ne izvzema iz odgovornosti (...) « .
Zgodovina medicine kljub temu spominja na okoliščine, ki so povzročile zlasti Nürnberški zakonik .
Odločitev pa je odvisna od suverenega spoštovanja sodnika.
Se nadaljuje…
Drugi odčitki (niso izčrpni)
"TRIBINA. Kar je zavrnjeno profesorju Didierju Raoultu, je dovoljeno drugim «( LE POINT , 7. junij 2020)
"Covid-19 in hidroksiklorokin:" empirizem ", zavrnjen profesorju Didierju Raoultu (v nujnih primerih), vendar tolerirajo" pediatrična zdravila "(v sedanji praksi)" ( CTIAP , 19. september 2020)
https://ctiapchcholet.blogspot.com/2021/01/le-vaccin-contre-la-covid-19.html
*
VSI MEDIJI SPREGLEDALI - tu je resnica o EU, cepivih in ivermectinu
Vprašanja EU Komisiji poslanke Evropskega parlamenta, Francesce Donato, z dne 25.8.2021
EU je izdala pogojno odobritev za uporabo cepiva COVID-19 v nujnih primerih, s šest-tedenskim preverjanjem podatkov o varnosti po cepljenju(1).
EUDRAVIGILANCE je doslej prejela približno 20.000 poročil o smrtnih primerih, verjetno povezanih s cepivi, in približno 700.000 poročil o neželenih učinkih, od tega 9 % hujše vrste. Vendar gre verjetno za podcenjevanje dejanskega obsega neželenih učinkov, saj ni aktivnega nadzora. Agencija EMA je pred kratkim posodobila seznam neželenih učinkov cepiv in dodala nove bolezni(2).
Poleg tega trend okužb med cepljenimi osebami v državah, kot sta Izrael in Združeno kraljestvo, kaže, da cepiva sama po sebi niso učinkovita proti različicam, ki trenutno prevladujejo.
Morebitne dolgoročne reakcije na cepiva mRNA, ki še nikoli niso bila odobrena za ljudi, ostajajo neznane(3).
Ali bo zaradi tega Evropska komisija:
1. preklicala ali začasno odvzela dovoljenje za uporabo teh cepiv zaradi pomanjkanja varnosti in učinkovitosti v smislu preprečevanja okužbe in okužbe z virusom SARS-CoV2;
2. dovolila uporabo zdravil, ki so se izkazala za učinkovita pri zdravljenju COVID-19, kot je ivermektin, in obsežnih protokolov za zgodnje zdravljenje na domu;
Vprašanja za EU Parlament: https://www.europarl.europa.eu/doceo/document/P-9-2021-003960_EN.html
EU je odobrila uslovno odobrenje za hitnu upotrebu vakcina protiv COVID-19, uz šestonedeljni pregled sigurnosnih podataka nakon vakcinacije.[1]
Do danas je EUDRAVIGILANCE primio oko 20 000 izvještaja o smrtnim slučajevima vjerovatno vezanim za vakcine i oko 700 000 neželjenih reakcija, od kojih je 9% teških. Ovi podaci su, međutim, potcijenjeni kada je u pitanju prava veličina štetnih efekata, s obzirom na to da ne postoji aktivan nadzor. EMA je nedavno ažurirala listu neželjenih reakcija na vakcine, dodajući nove bolesti. [2]
Štaviše, trend infekcija među vakcinisanim ljudima u zemljama poput Izraela i Velike Britanije pokazuje da same vakcine nisu efikasne protiv varijanti koje trenutno prevlađuju.
Moguće dugotrajne reakcije na vakcine protiv mRNK, koje nikada ranije nisu bile odobrene za ljude, ostaju nepoznate. [3]
S obzirom na to, hoće li Komisija:
- povući ili suspendovati odobrenje za upotrebu tih vakcina zbog nedostatka zahtjeva za sigurnošću i efikasnošću u smislu sprečavanja infekcije i zaraze virusom SARS-CoV2;
- odobri upotrebu lijekova koji su se pokazali efikasnim u liječenju COVID-19, kao što je ivermektin, i velikih protokola za rano liječenje kod kuće;
- uspostaviti sistem aktivnog nadzora za vakcinisane osobe, pružajući im podršku i olakšavajući neophodan tretman za neželjene efekte?
[1] Na kraju „primarnog završetka“ ispitivanja, nije predviđena mogućnost prikupljanja ili dostavljanja podataka o „štetnim efektima“. EMA je navela da će nakon izdavanja dozvole za promet vakcina vakcinirane osobe u cijeloj Evropi morati biti nadgledane najmanje godinu dana kako bi se dokumentovale sve zakašnjele neželjene reakcije.
[2] Pogledajte: https://www.ema.europa.eu/en/human-regulatory/overview/public-health-threats/coronavirus-disease-covid-19/treatments-vaccines/vaccines-covid-19/covid-19-vaccines-authorised#safety-updates-for-authorised-covid-19-vaccines-section
[3] BioNTech/Pfizer i Moderna vakcine koriste ovu tehniku, što bi zahtijevalo mnogo duže vremena za procjenu prije nego što se da cjelokupnoj populaciji.
*
Razlog: cjepiva koja se koriste od 27. prosinca 2020. ilegalni su proizvod jer nisu u skladu s uvjetnim odobrenjem za stavljanje u promet
“U Francuskoj sudska blokada cijepljenja od 26. kolovoza…“ Dobro ste pročitali – ovo je iznimno važna vijest koja je prešućena u svim vodećim, tzv. mainstream medijima. Ipak, vijest se uspjela probiti u javnost zahvaljujući hrabrim ljudima koji nesebično i marljivo rade za dobrobit svakog čovjeka kao i za otkrivanje istine u svezi pandemije COVID-19 i svega što je povezano s njom, a u prvom redu to je nametnuto i prisilno cijepljenje eksperimentalnim cjepivom protiv COVID-19.
„Zaista sam iznenađen(a) što ne vidim nikakve komentare u vezi sa skraćenim sudskim postupcima/istragama protiv ANSM-a, CNOM-a, CNOP-a, Vidala za upotrebu neovlaštenih proizvoda, a koje je uspostavilo francusko udruženje „Réaction 19“, kojem predsjeda odvjetnik Carlo Alberto Brusa.“
Ovaj skraćeni sudski postupak bit će objavljen prije sudskog izlaganja u Parizu 21. listopada 2021. A to nije daleko. Razlog: cjepiva koja se koriste od 27. prosinca 2020. ilegalni su proizvod jer nisu u skladu s uvjetnim odobrenjem za stavljanje u promet koje je proizvođačima dodijelila Europska komisija. Od navedenog datuma početka cijepljenja, u Francuskoj su sve injekcije (cjepiva) vršene s ilegalnim proizvodima. Sve naknade socijalnog osiguranja također su nezakonite.
Trenutačni postupak zahtijeva da se ODMAH ZAUSTAVE sva cijepljenja. Vrijeme je da mediji odrade svoj posao informiranja javnosti jer su svi primili priopćenje za javnost još 27. kolovoza 2021. iz „Réaction 19“ koju je potpisao njezin predsjednik Brusa. I mi moramo učiniti svoj dio posla jer se od danas nitko ne smije cijepiti, što može biti osiguranje za sve one koji su se bojali da će to morati učiniti kako bi sačuvali svoja radna mjesta ili, još gore, morali cijepiti svoju djecu. Što više širimo te informacije, prije će cijepljenje prestati. Onog trenutka kada saznamo za ovaj postupak, odgovorni smo za svako daljnje cijepljenje.
„Ne oslanjajmo se na medije da će širiti ovaj glas, već uzmimo jedni druge za ruku i ‘preplavimo’ svoje kontakte, susjede, liječničke ordinacije, ljekarne u susjedstvu itd., jer tko bi se usudio nastaviti ilegalno cijepiti nakon što je saznao ovu činjenicu? Zakonske kazne bit će stroge i nitko ih ne će izbjeći.“
Napomena:
U ovom gore navedenom kratkom tekstu spominju se neke francuske medicinske skupine čiji nazivi su akronimi. Ovdje dajemo pojašnjenje:
ANSM – Nacionalna agencija za sigurnost medicinskih i zdravstvenih proizvoda. Ima nadležnost nad farmakološkim i biološkim proizvodima, medicinskim uređajima itd.
CNOM – Francusko liječničko vijeće, ‘red liječnika’.
CNOP – Francuski red ljekarnika.
Vidal – „Vidal France“ bavi se informacijama i savjetima/preporukama o zdravstvenim proizvodima i medicinskim uređajima. Osim toga, François Molins, državni tužitelj Kasacijskog suda u Francuskoj potvrdio je kako je „Sud pravde“ (Cour de Justice de la République) primio tisuće (pri)tužbi protiv francuskih ministara i drugih visokih državnih dužnosnika, uključujući i one iz zdravstvenog i javnozdravstvenog sektora, zbog načina vladinog upravljanja COVID krizom. Naime, to je jedini Sud u Francuskoj koji može procesuirati i suditi premijere, ministre, državne tajnike i druge visoke državne dužnosnike.
Naprijed navedena ‘obavijest od najveće važnosti’ o sudskoj blokadi cijepljenja protiv COVID-19 u Francuskoj podudara se s izjavama odvjetnice Renate Holzeisen. Naime, Senta Depuydt, predsjednica „Children’s Health Defense Europe“ razgovarala je s Renatom Holzeisen. Videozapis i transkript velikog razgovora u kojem je odvjetnica Holzeisen vrlo detaljno obrazložila sve najznačajnije ozbiljne pravne „propuste“ u svezi pandemije, cjepiva i cijepljenja u cijelosti je objavljen na internetskoj stranici organizacije „Children’s Health Defense Europe“ pod naslovom: „Covid Vaccines Violate European Legislation“ („Cjepivima protiv COVID-19 krši se europsko zakonodavstvo“).
Odvjetnica Renate Holzeisen iz Južnog Tirola u Italiji „rješava pitanja cjepiva protiv COVID-19 na razini europskih institucija i radi na poništenju uvjetnih odobrenja za sva četiri genska cjepiva protiv COVID-19.“ Renate Holzeisen surađuje sa svojim njemačkim i austrijskim kolegama uključujući i suradnju s pravnim stručnjakom dr. Reinerom Füllmichom. Ona je ujedno i članica Savjetodavnog odbora u ‘Children’s Health Defense Europe.’ Renate Holzeisen je visoko obučena odvjetnica u području ekonomskih i fiskalnih pitanja. Podnijela je impresivan broj slučajeva povezanih s cjepivima protiv COVID-19.
Renate Holzeisen u razgovoru, između ostalog, izjavila je sljedeće: „Utvrdili smo da su savjetovanja/vijećanja koja je poduzela Europska komisija u osnovi protivna europskom zakonu o uvjetnoj autorizaciji (odobrenju) lijekova i cjepiva, ako se radi o cjepivima, za koja znamo da su proizvodi genske terapije. One (odluke) moraju se donijeti u skladu s europskom uredbom 507 iz 2006. I jedan od uvjeta koje je odredio europski zakonodavac je da proizvod mora jamčiti pozitivnu ravnotežu između koristi i rizika. Prije svega moramo objasniti da ove supstance nisu ispitane i odobrene za sprječavanje infekcije/zaraze virusom SARS-CoV-2. One su samo ispitane i odobrene za prevenciju bolesti COVID-19.
I tu već vidimo mnogo toga, ne samo nesporazuma, nego zapravo, prave propagande, dezinformirajuće propagande institucija i europskih vlada. A to je vrlo neprihvatljiva okolnost. To sada vidimo sa zakonima koji su objavljeni u različitim europskim zemljama poput Francuske i Italije u vezi s takozvanim Zelenim putovnicama (COVID putovnice ili propusnice, op.a.)…
Nikada nisu proglasili odobrenje za sprječavanje infekcije jer sama EMA (Europska agencija za lijekove, op.a.) izjavljuje da apsolutno NIJE dokazano da ove tvari djeluju na sprječavanju infekcije. Stoga Europska komisija nije mogla odobriti ove 4 tvari koje su Cominarty (Pfizer/BioNTech), Moderna čije cjepivo se sada naziva Spikevax, cjepivo ‘AstraZenece’ koje se sada zove Vaxzevria i cjepivo Janssen ili Johnson & Johnson. Nemaju autorizaciju/odobrenje za sprječavanje infekcije virusom i to je pravno obvezujuće. Dakle, ovo zakonodavstvo je već zakazalo/ propalo prije nego što je uvedeno. I mi, odvjetnici, sada radimo na tome, jer je jasno da bismo imali apsolutno protuustavnu diskriminaciju među ljudima koji nisu tretirani ovim pokusnim tvarima u odnosu na cijepljene osobe. Čak ni ljudi koji su tretirani / ‘liječeni’ ovim tvarima, nisu bili cijepljeni u svrhu sprječavanja infekcije. …“
Transkript cijelog razgovora s odvjetnicom Renatom Holzeisen možete pročitati na internetskoj stranici Children’s Health Defense Europe.
Nadam se da će netko od hrvatskih odvjetnika koji u velikoj većini šute, pročitati transkript ovog itekako značajnog razgovora i za dobrobit svakog hrvatskog čovjeka, pridružiti se zajedno s građanima pokrenutim pravnim radnjama kao tzv. umješači.
Izvor:
- Profession Gendarme: „La vaccination est bloquée par voie judiciaire depuis le 26 août dernier…“, 5. 9. 2021.; www.profession-gendarme.com
- L’association Réaction 19: https://reaction19.fr
- „Gestion de la pandémie: »des milliers de plaintes« arrivent à la Cour de justice de la République“ 5. 9. 2021.; https://francais.rt.com/france/
- Childrens’s Health Defense Europe: videozapis i transkript razgovora s Renate Holzeisen: „COVID Vaccines Violate European Legislation“; https://childrenshealthdefense.eu/aiovg_videos/
Rodjena Marija Kuhar, dr. vet. med.
*
Peter Doshi BJM: https://blogs.bmj.com/bmj/2021/08/23/does-the-fda-think-these-data-justify-the-first-full-approval-of-a-covid-19-vaccine/
*
Pfizer research organization falsified data in their Phase III COVID-19 vaccine trial results and fired those who complained about unethical trial practices to the FDA, according to a BMJ investigation, citing a whistleblower.
https://www.bmj.com/content/375/bmj.n2635
*
Znanstveniki tožijo FDA za podatke, na osnovi katerih so odobrili Pfizer cepivo:
World Council for Health Calls for an Immediate Stop to the Covid-19 Experimental “Vaccines”
A. CONSENSUS OF WORLD’S FOREMOST EXPERTS
Globally renowned experts, including Dr. Paul Alexander, Dr. Byram Bridle, Dr. Geert Vanden Bossche, Prof. Dolores Cahill, and Drs. Sucharit Bhakdi, Ryan Cole, Richard Fleming, Robert W. Malone, Peter McCullough, Mark Trozzi, Michael Yeadon, Wolfgang Wodarg, and Vladimir Zelenko, among many others, consistently warn the world about the adverse effects resulting from Covid-19 experimental injections; they also warn about their longterm effects, which cannot be known at this time since most clinical trials will be not completed until 2023, and some as late as 2025.
In June 2021, Dr. Tess Lawrie, co-founder of the World Council for Health and member of the Council’s Steering Committee, courageously described the global crisis and called for urgent action: “There is now more than enough evidence on the [UK] Yellow Card system to declare the COVID-19 vaccines unsafe for use in humans. Preparation should be made to scale up humanitarian efforts to assist those harmed by the COVID-19 vaccines and to anticipate and ameliorate medium to longer term effects.”
B. DECLARATION
The World Council for Health declares that it is time to put an end to this humanitarian crisis. Further, the Council also declares that any direct or indirect involvement in the manufacturing, distribution, administration and promotion of these injections violates basic principles of common law, constitutional law and natural justice, as well as the Nuremberg Code, the Helsinki Declaration, and other international treaties.
C. UNCENSORED FACTS
We now know that children are over one hundred times more likely to die from these experimental injections than Covid-19. Injected athletes, globally, are collapsing before our very eyes. In spite of the fact that reporting systems are limited and passive, millions of adverse effects have been recorded, which include death, paralysis, blood clots, strokes, myocarditis, pericarditis, heart attacks, spontaneous miscarriage, chronic fatigue and extreme depression.
See: coronavirus-yellowcard.mhra.gov.uk
See: vaers.hhs.gov
See: ema.europa.eu/en/human-regulatory/researchdevelopment/pharmacovigilance/eudravigilance
See: vigiaccess.org (search covid-19 vaccine)
D. VICTIM TESTIMONIES
The World Council for Health acknowledges and respects the experiences and testimony of the victims of this worldwide medical experiment. We also declare and confirm that safe, effective and affordable treatments for Covid-19 exist and should be made available to all who need them.
See: wewanttobeheard.com
See: nomoresilence.world
See: vaxtestimonies.org/en
E. NOT SAFE, NOT EFFECTIVE
Recent studies confirm the risks associated with Covid-19 experimental injections. Emerging research establishes that the injections are neither safe nor effective, and, in fact, are toxic. While some of the known ingredients of the injections cause biological harm, it is even more concerning that the unknown and undisclosed ingredients may present an even greater threat to human health.
F. CEASE AND DESIST
The World Council for Health is ethically and lawfully bound to issue this Declaration, demanding that governments and corporations cease and desist from direct or indirect participation in the manufacturing, distribution, administration or promotion of Covid-19 experimental injections.
The Council declares that every living man and woman has a moral and legal duty to take immediate and decisive action to halt this unprecedented medical experiment, which continues to cause unnecessary and immeasurable harm.
G. NOTICE OF LIABILITY
The right of bodily integrity and the right to informed consent are inalienable and universal human rights, which have been trampled by government mandates and corporate imperatives. Thus, the World Council for Health declares that any person or organization directly or indirectly participating in the manufacturing, distribution, administration or promotion of Covid-19 experimental biologics will be held liable for the violation of principles of justice grounded in civil, criminal, constitutional and natural law, as well as international treaties.
Mar 14, 2021